
����Ŀ��(I)���������ʽ��з���:��H��D��O2��O3���Ҵ�(C2H5OH)�����(CH3-O-CH3)�����������춡���C60����ʯ
(1)��Ϊͬλ�ص���_______(���š���ͬ)��
(2)��Ϊͬ�����������_______ ��
(3)��Ϊͬ���칹�����________��
(II)��ӦFe + H2SO4=== FeSO4+ H2���������仯������ͼ��ʾ:
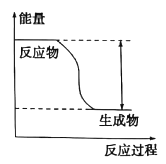
(1)�÷�ӦΪ _______��Ӧ(����ȡ����ȡ�)��
(2)��Ҫʹ�÷�Ӧ�ķ�Ӧ���ʼӿ죬���д�ʩ���е���______(����ĸ)��
A.����ƬΪ���� B. ��ϡ����Ϊ98%��Ũ���� C.�ʵ������¶�
(3)����������Ӧ��Ƴ�ԭ��أ�ͭΪԭ���ijһ�����ϣ���ͭΪ_____(���������)�����ü��Ϸ����ĵ缫��ӦΪ___________��
���𰸡� �� �ڢ� �ۢ� ���� AC �� 2H++2e-==H2��
��������
(I)��1��������ͬ����������ͬ����������ͬ��������ͬһԪ�صIJ�ͬ���ػ�Ϊͬλ�أ���2��ͬ��Ԫ����ɵIJ�ͬ�ֵ��ʻ�Ϊͬ������������3��������ͬ����ʽ���ṹ��ͬ�Ļ����ﻥΪͬ���칹�壮
(II)��1�����ݷ�Ӧ���������������ϵ��������2������������������ʵ�Ӱ���������3��ͭ������ϡ���ṹ�ɵ�ԭ����У�����ʧ������������ͭ��������������ʧ���ӷ���������Ӧ�������ϵõ��ӷ�����ԭ��Ӧ��
(I)��1��H��D����������ͬ����������ͬ����Ϊͬλ�أ���ѡ�٣���2����O2��O3����C60����ʯ��ͬ��Ԫ����ɵIJ�ͬ�ֵ��ʣ���ѡ�ڢ�����3���Ҵ���C2H5OH������ѣ�CH3-O-CH3���������飨CH3CH2 CH2 CH3�����춡�飨CH3-CH��CH3��2����ʽ��ͬ���ṹ��ͬ����Ϊͬ���칹�壬��ѡ�ۢܣ�
(II)��1����ͼ���֪����Ӧ�����������������������������Ը÷�ӦΪ���ȷ�Ӧ����2��A������ƬΪ���ۣ������˽Ӵ��������Ӧ��������A��ȷ��B����Ӧ��Ϊ�������ᷴӦ����ϡ����Ϊ98%��Ũ���� �������ۻ�����������������B����C�������¶ȣ���Ӧ��������C��ȷ����ѡAC����3��ͭ������ϡ���ṹ�ɵ�ԭ����У�����ʧ���ӷ���������Ӧ���������������ϵ缫��ӦʽΪFe-2e��=Fe2����ͭ�������������������ӵõ��ӷ�����ԭ��Ӧ���缫��ӦʽΪ2H��+2e��=H2����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����0.25Ħ���������У����е���ԭ�Ӹ���ԼΪ
A.1B.0.25C.6.02��1023D.5��1023
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������[KAl��SO4��2��12H2O]���������������й㷺��;������ˮ�ľ�������ֽ��ҵ����ʩ������ʳƷ��ҵ�ķ��ͼ��ȣ������������ķ��ϩ����ң���Al��Al2O3������SiO2��FeO��xFe2O3�����Ʊ������������������£�
�ش��������⣺
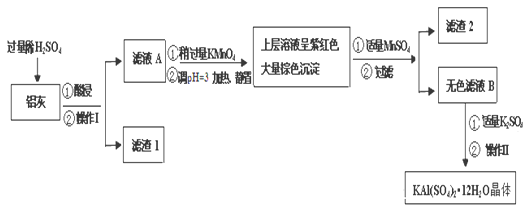
��1��������ˮ��ԭ���ǣ������ӷ��̱�ʾ��________________��
��2����������________��������������Ũ����________�����ˡ�ϴ�ӡ����
��3��������ҺA���Ƿ����Fe2+���Լ���________��ֻ��һ���Լ���
��4������ҺA�м��������ط�����Ӧ�����ӷ���ʽΪ����������Fe2+ ת��ΪFe3+��MnO4��ת��ΪMn2+��________________��
��֪�������������������pH���±���ʾ
Al��OH��3 | Fe��OH��2 | Fe��OH��3 | |
��ʼ����ʱ | 3.4 | 6.3 | 1.5 |
��ȫ����ʱ | 4.7 | 8.3 | 2.8 |
ע���������ӵ���ʼŨ��Ϊ0.1mol��L��1
���ݱ������ݽ��͵�pH=3��Ŀ��________________��
��5����֪����pH=3�����������£�MnO4������Mn2+��Ӧ����MnO2������MnSO4������Ӧ�����ӷ���ʽΪ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ���ǣ�������
A. �����£���ˮ�м������������������ƣ�c(H+)����Kw���
B. 0.1 mol��L-1�Ĵ����ˮϡ�ͣ�c(CH3COOH)/c(CH3COO��)��С����K������
C. ���������pH����ͬ�Ĵ����������ȫ�ܽ������þ�ۣ�������������ʱ��
D. 25������AgCl����Һ�м�������NaCl������c(Ag+)��С��Ksp(AgCl)��С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к��зḻ����������ʽ���ڵĵ�Ԫ�ء���ͼ��ʵ���ҴӺ�������ȡ������̵�һ���֡�
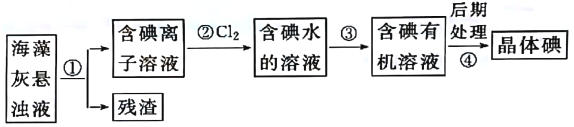
�����ж���ȷ����
A. ����١��۵IJ����ֱ��ǹ��ˡ���ȡ��Һ
B. ����ڵķ�Ӧ�Ƿ�������ԭ��Ӧ
C. ������м�����л��ܼ������Ǽ�ϩ�����Ȼ�̼
D. ����ܵIJ����ǹ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
(��)ij̽��С����HNO3�����ʯ��Ӧ������������С�ķ������о�Ӱ�췴Ӧ���ʵ����ء�����HNO3Ũ��Ϊ1.00mol/L��2.00mol/L������ʯ��ϸ�����ʹֿ������ֹ��ʵ���¶�Ϊ25�桢35�棬ÿ��ʵ��HNO3������Ϊ25.00mL������ʯ����Ϊ10.00g��
���������ʵ����Ʊ�������ʵ��Ŀ��һ������գ�
ʵ�� ��� | �¶� ���棩 | ����ʯ ��� | HNO3Ũ�ȣ�mol/L�� | ʵ��Ŀ�� |
�� | 25 | �ֿ��� | 2.00 | (I)ʵ��ٺ͢�̽��Ũ�ȶԷ�Ӧ���ʵ�Ӱ�죻 (II)ʵ��ٺ͢�̽���¶ȶԷ�Ӧ���ʵ�Ӱ�죻 (III)ʵ��ٺ͢�̽��______________�Է�Ӧ���ʵ�Ӱ�� |
�� | 25 | �ֿ��� | _______ | |
�� | _____ | �ֿ��� | 2.00 | |
�� | 25 | ϸ���� | 2.00 |
(��)��2.5 mol A��2.5 mol B��Ϸ���2 L�ܱ������������Ӧ��3A(g)��B(g)![]() xC(g)��2D(g)����5 s��Ӧ��ƽ�⡣�ڴ�5 s��C��ƽ����Ӧ����Ϊ0.2 mol/(L��s)��ͬʱ����1 mol D������
xC(g)��2D(g)����5 s��Ӧ��ƽ�⡣�ڴ�5 s��C��ƽ����Ӧ����Ϊ0.2 mol/(L��s)��ͬʱ����1 mol D������
��1����ƽ��ʱB��ת����Ϊ_____________________��
��2��x��ֵΪ___________________��
��3�����¶Ȳ��䣬��ƽ��ʱ�����������ѹǿ�Ƿ�Ӧǰ��____________����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10.0 mL 0.10 mol/L��ˮ�е���0.10 mol/L�����ᣬ��Һ��pH����������������ϵ��ͼ��ʾ(�����������ݳ�)�������й�������ȷ����( )
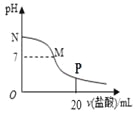
A. M��N��һ�����ڣ�c(Cl��)>c(NH4+)>c(OH��)>c(H+)
B. M���Ӧ���������Ϊ10.0mL
C. pH=7����Һ�У�c(NH4+)=c(Cl��)=c(H+)=c(OH��)
D. P�㴦����Һ�д��ڣ�2c(NH4+)+2c(NH3��H2O)=c(Cl��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���縡ѡ���۷��ǹ�ҵ�ϲ��õ�һ����ˮ������������������ˮ��pH��5.0��6.0֮�䣬ͨ���������Fe(OH)3���壬Fe(OH)3��������������ã�������ˮ�е������ʹ�������������ˮ�����ã���ԭ����ͼ��ʾ������˵����ȷ����
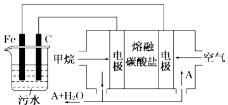
A��ʯī�缫�Ϸ���������Ӧ
B������ͼʾ������AΪCO2
C��Ϊ��ǿ��ˮ�ĵ���������������ˮ�м��������Ҵ�
D������ȼ�ϵ����CO32�������һ���ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��[ѡ��5-�л���ѧ����]�л���F��һ����Ҫ�ľ�ϸ�����ϳ��м��壬��ϳ���·��ͼ:
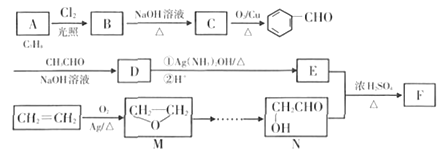
��֪: ![]() ���ش���������:
���ش���������:
(1)�л���A��C�����Ʒֱ�Ϊ______��_____��D![]() E�ķ�Ӧ����Ϊ__________��
E�ķ�Ӧ����Ϊ__________��
(2)�л���F�Ľṹ��ʽΪ________��д��B ![]() C��Ӧ����ʽ__________��
C��Ӧ����ʽ__________��
(3)�л���D�к��������ŵ�����Ϊ_______,��Ҫ֤��D�к��С�![]() ��������,ʵ�鷽��Ϊ_______��
��������,ʵ�鷽��Ϊ_______��
(4)E��ͬ���칹���ж���,�������ڷ����廯�������ʹ������Ȼ�̼��Һ��ɫ,����������������Һ�з���ˮ�ⷴӦ��ͬ���칹����__________�֡�
(5)��������(![]() )��һ����Ҫ��ʯ����Ʒ����ѧ���ʻ���,����ˮ��±���⡢�Ҵ��Ⱥܶ�����a�������ӳɷ�Ӧ��д����M
)��һ����Ҫ��ʯ����Ʒ����ѧ���ʻ���,����ˮ��±���⡢�Ҵ��Ⱥܶ�����a�������ӳɷ�Ӧ��д����M![]() N�ĺϳ�·��:____________��
N�ĺϳ�·��:____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com