
某水溶液只可能含有K+、Al3+、Fe3+、Mg2+、Ba2+、NH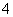 、Cl-、CO
、Cl-、CO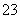 、SO
、SO 中的若干种离子。某同学取100 mL的溶液分成两等份进行如下实验:
中的若干种离子。某同学取100 mL的溶液分成两等份进行如下实验:
①第一份加过量的氢氧化钠溶液后加热,收集到0.02 mol的气体,无沉淀产生,同时得到溶液甲。
②向溶液甲中通过量的二氧化碳气体,生成白色沉淀,沉淀经过滤,洗涤灼烧后,得到1.02 g固体。
③第二份加足量的氯化钡溶液后,生成白色沉淀,沉淀经盐酸充分洗涤,干燥,得到11.65 g固体。
据此,该同学得到的结论正确的是( )
A.实验①中产生的气体为氨气,并可得原溶液中c(NH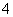 )=0.2 mol·L-1
)=0.2 mol·L-1
B.实验③中的白色沉淀中一定有BaSO4,无BaCO3
C.原溶液中一定有K+,且c(K+)=0.4 mol·L-1
D.若要判断原溶液中是否有Cl-,无需另外设计实验验证
答案 B
解析 由①得50 mL溶液中n(NH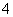 )=0.02 mol,根据离子共存原则,无Fe3+、Mg2+。②中得到的沉淀为Al(OH)3,1.02 g固体为Al2O3,则50 mL溶液中n(Al3+)=0.02 mol,根据离子共存原则,无CO
)=0.02 mol,根据离子共存原则,无Fe3+、Mg2+。②中得到的沉淀为Al(OH)3,1.02 g固体为Al2O3,则50 mL溶液中n(Al3+)=0.02 mol,根据离子共存原则,无CO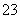 。由③得,溶液中一定含SO
。由③得,溶液中一定含SO ,其物质的量为n(SO
,其物质的量为n(SO )=0.05 mol(指50 mL溶液中),根据离子共存原则,原溶液中一定无Ba2+。综上所述,有SO
)=0.05 mol(指50 mL溶液中),根据离子共存原则,原溶液中一定无Ba2+。综上所述,有SO (0.05 mol),Al3+(0.02 mol),NH
(0.05 mol),Al3+(0.02 mol),NH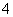 (0.02 mol),根据电荷守恒,还一定有K+,根据上述实验,由于无法确定Cl-,所以 n(K+)≥0.05 mol×2-0.02 mol×3-0.02 mol=0.02 mol,其浓度为c(K+)≥
(0.02 mol),根据电荷守恒,还一定有K+,根据上述实验,由于无法确定Cl-,所以 n(K+)≥0.05 mol×2-0.02 mol×3-0.02 mol=0.02 mol,其浓度为c(K+)≥ =0.4 mol·L-1。
=0.4 mol·L-1。


 轻松暑假总复习系列答案
轻松暑假总复习系列答案科目:高中化学 来源: 题型:
某烃类化合物A的质谱图表明其相对分子质量为84,红外光谱表明分子中含有碳碳双键,核磁共振氢谱表明分子中只有一种类型的氢。
(1)A的结构简式为___________________________________________________。
(2)A中的碳原子是否都处于同一平面?________(填“是”或“不是”)。
(3)在下图中,D1、D2互为同分异构体,E1、E2互为同分异构体。
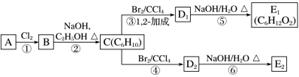
反应②的化学方程式为____________________________________________;C的化学名称是
______________;E2的结构简式是__________________;④、⑥的反应类型依次__________、__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用一带静电的玻璃棒靠近A、B两种纯液体流,根据图分析,这两种液体分子的极性正确的是( )
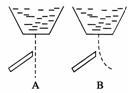
A.A是极性分子,B是非极性分子
B.A是非极性分子,B是极性分子
C.A和B都是极性分子
D.A和B都是非极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D、E五种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有两个不成对的电子;D、E原子核内各自的质子数与中子数相等;B元素可分别与A、C、D、E生成RB2型化合物,并知:在DB2中D与B的质量比为7∶8,在EB2中E与B的质量比为1∶1。试回答:
(1)写出D原子的电子排布式:________________。
(2)B、C两元素的第一电离能较大的元素是______(填写元素符号)。
(3)C的氢化物的空间结构为________,C与氢形成的离子化合物CH5的电子式是
______________。
(4)C的单质中π键的数目为________,B、D两元素的气态氢化物的稳
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1 NaOH溶液:K+、Na+、SO 、CO
、CO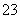
B.0.1 mol·L-1 Na2CO3溶液:K+、Ba2+、NO 、Cl-
、Cl-
C.0.1 mol·L-1 FeCl3溶液:K+、NH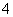 、I-、SCN-
、I-、SCN-
D.c(H+)/c(OH-)=1×1014的溶液:Ca2+、Na+、ClO-、NO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能够大量共存的是( )
A.NH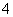 、NO
、NO 、Na+、SO
、Na+、SO
B.H+、Fe2+、Na+、NO
C.Ba2+、K+、Al3+、HCO
D.NH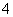 、Li+、OH-、SO
、Li+、OH-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
镁、铝单质的化学性质以相似为主,但也存在某些重大差异性,下列物质能用于证明二者存在较大差异性的是( )
A.CO2 B.盐酸
C.NaOH溶液 D.水
查看答案和解析>>
科目:高中化学 来源: 题型:
铝是一种应用广泛的金属,工业上用Al2O3和冰晶石(Na3AlF6)混合熔融电解制得。
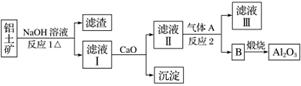
①铝土矿的主要成分是Al2O3和SiO2等。从铝土矿中提炼Al2O3的流程如下:
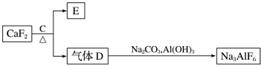
②以萤石(CaF2)和纯碱为原料制备冰晶石的流程如下:
回答下列问题:
(1)写出反应1的化学方程式_______________________________________________________。
(2)滤液Ⅰ中加入CaO生成的沉淀是________,反应2的离子方程式为________________________________________________________________________。
(3)E可作为建筑材料,化合物C是________,写出由D制备冰晶石的化学方程式________________________________________________________________________。
(4)电解法制铝的化学方程式是________,以石墨为电极,阳极产生的混合气体的成分是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com