
【题目】在一定条件下,对于密闭容器中进行的反应2NO2(g)![]() 2NO(g)+O2(g),下列说法中,能充分说明该反应已经达到化学平衡状态的是
2NO(g)+O2(g),下列说法中,能充分说明该反应已经达到化学平衡状态的是
A.反应混合物中NO2、NO、O2的物质的量之比为2:2:1B.v(NO2)=2v(O2)
C.混合气体的颜色不改变D.生成O2的速率与生成NO2的速率相等
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】在我国的资源储备中,铬是重要的战略金属资源。以下是以某铬渣(主要成分为Cr2O3,杂质主要是FeO、SiO2等)为原料生产Cr2O3的工艺流程:

已知:Ksp[Mg(OH)2]=1.8×10-11,Ksp[Cr(OH)3]=6.4×10-31。
(1)若以氧化物形式表示矿物的组成,则Fe2SiO4可表示为____________。
(2)焙烧时通入氧气的作用是__________________________________________
(3)“除杂”时加入MgSO4-(NH4)2SO4混合物与溶液中少量的PO43-、AsO43-、SiO32-反应,使其分别转化为NH4MgPO4、NH4MgAsO4、MgSiO3沉淀除去。测得反应pH与除杂率的关系如图所示。

①反应过程中控制溶液pH为9,pH>9时除杂率降低的原因是_________。
②反应的温度控制在80 ℃左右,温度不宜太高的主要原因是___________。
(4)“还原”时先调节溶液pH,再加入焦亚硫酸钠(Na2S2O5)。
①完成“还原”反应的离子方程式:________Cr2O72-+________S2O32-+________===________Cr3++________SO42-+________
②已知铬液中c(Cr2O72-)=0.32 mol·L-1,为了不在还原过程中产生Cr(OH)3沉淀,应控制溶液的pH不大于________。
(5)“沉铬”的主要副产物为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在有关限定条件下溶液中一定能大量共存的是( )
A. 由水电离产生的c(H+)=10-12mol/L的溶液中:K+、Na+、ClO-、I-
B. c(H+)=![]() mol/L的溶液中:K+、Fe3+、Cl-、CO32—
mol/L的溶液中:K+、Fe3+、Cl-、CO32—
C. 常温下,![]() =1×10-12的溶液:K+、AlO2—、CO32—、Na+
=1×10-12的溶液:K+、AlO2—、CO32—、Na+
D. pH=13的溶液中:AlO2—、Cl-、HCO3—、SO42—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用0.10mol·L-1NaOH溶液分别滴定20.00mL浓度均为0.10 mol·L-1CH3COOH
溶液和HCN溶液所得滴定曲线如右图。下列说法正确的是

A. 点①和点②所示溶液中:c(CH3COO-)<c(CN-)
B. 点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C. 点①和点②所示溶液中:c(CH3COO-)-c(CN-)=c(HCN)-c(CH3COOH)
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定量的有机物充分燃烧后的产物通入足量的石灰水中完全吸收,经过滤、洗涤、干燥得沉淀20g, 滤液质量比原石灰水减少7.6g,该有机物可能是( )
A.乙炔B.乙烷C.乙二醇D.乙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有物质的量浓度均为![]() 的①
的①![]() 溶液 ②
溶液 ②![]() 溶液③
溶液③ ![]() 溶液各25mL,下列说法正确的是
溶液各25mL,下列说法正确的是
A.3种溶液pH的大小顺序是③>②>①
B.若将3种溶液稀释相同倍数,pH变化最大的是①
C.若分别加入25mL ![]() 盐酸后,pH最小的是②
盐酸后,pH最小的是②
D.若升高温度,则③的pH不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 0.1 mol/LC6H5ONa溶液中:c(Na+)>c(C6H5O-)>c(H+)>c(OH-)
B. Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小
C. pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等
D. 在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B两个完全相同的装置,某学生分别在它们的侧管中装入![]()
![]() 和
和![]()
![]() ,A、B中分别有10mL相同浓度的盐酸(不考虑盐酸的挥发),将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )
,A、B中分别有10mL相同浓度的盐酸(不考虑盐酸的挥发),将两个侧管中的物质同时倒入各自的试管中,下列叙述正确的是( )

A.B装置的气球膨胀的体积大
B.最终两试管中NaCl的物质的量一定相同
C.若最终两气球体积不同,则盐酸的浓度一定小于或等于![]()
D.若最终两气球体积相同,则盐酸的浓度一定大于或等于![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】敌草胺是一种除草剂。它的合成路线如下:
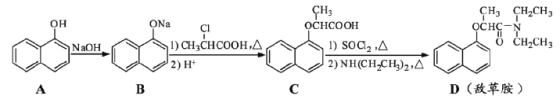
回答下列问题:
(1)在空气中久置,A由无色转变为棕色,其原因是______________________。
(2)C分子中不能与金属钠反应的官能团是______________________(填名称)。
(3)C转化为D的第一步反应有SO2生成,写出该反应的化学方程式______________。
(4)同时满足下列条件的C的同分异构体有______种。
①能与金属钠反应放出H2
②是萘的衍生物,且取代基都在同一个苯环上
③可发生水解反应,其中一种水解产物能发生银镜反应,另一种水解产物分子中有5种不同化学环境的氢
(5)若C不经提纯,产物敌草胺中将混有少量副产物E,E是一种由B和C生成的酯(变化过程中碳原子数未变),则E的分子式为___________________。
(6)已知:![]() ,若以苯酚和乙酸为原料制备
,若以苯酚和乙酸为原料制备![]() ,其合成路线为______________________。
,其合成路线为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com