
【题目】下列物质中,主要成分不是SiO2的是
A. 硅酸 B. 玛瑙 C. 水晶 D. 石英
 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.石油的催化重整和煤的干馏均可以得到芳香烃,说明石油和煤中含有芳香烃
B.石油裂解的目的主要是为了得到更多的汽油
C.石油分馏得到的产物可用来萃取溴水中的溴
D.石油裂化主要得到的是乙烯、丙烯等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期金属元素甲~戊在元素周期表中的相对位置如右表所示,下面判断正确的是
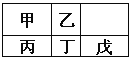
A. 原子半径:丙<丁<戊
B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊
D. 最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质氧化性、还原性的强弱,不仅与物质的结构有关,还与浓度和反应温度有关,下列各组物质由于浓度不同而发生不同反应的是:
A. Cu与HNO3 B. Cu与FeCl3 C.Zn与HCl D.FeCl3与NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
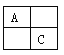
(1)D的离子结构示意图为_____________。
(2)B、C、D形成的简单离子半径由大到小的顺序: > > (写离子符号)
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到60 mL 10.0 mol/L乙的浓溶液中,充分反应,共收集到4.48L(标准状况)气体,则该气体的成分是_________,反应中电子转移数为____________。若使上述中反应后剩余的铜片继续溶解,可向其中加入稀硫酸,写出反应的离子方程式: 。
(4)将两份足量的B单质分别加入到等体积等浓度的硫酸和NaOH溶液中,充分反应生成气体的体积比为__________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】淀粉水解的产物(C6H12O6)用硝酸酸化可以制备草酸(H2C2O4),装置如图所示:
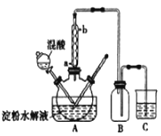
实验过程如下:
①将1:1的淀粉水乳液与少许98%硫酸加入烧杯中,水浴加热30 min;
②将一定量的淀粉水解液加入三颈烧瓶中;
③在5560℃条件下,缓慢滴加混酸(65%HNO3与98%H2S04的质量比为4 : 3)溶液;
④反应3h左右,冷却、过滤后再重结晶得二水合草酸晶体(H2C2O4·2H2O)。
硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3=3H2C2O4+9NO2↑+3NO↑+9 H2O
C6H12O6+8HNO3=6CO2↑+8NO↑+10H2O
C6H12O6+2HNO3=6CO2↑+2NO↑+4H2O
请回答下列问题:
(1)实硷①加入98%硫酸少许的目的是_____________。
(2)检验淀粉是否水解完全所用的试剂为____________。
(3)冷凝水的进口是_______(填“a”或“b”)。
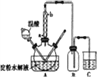
(4)装置B的作用为___________。
(5)实验中若混酸滴加过快,将导致草酸产量下降,其原因是______________。
(6)当尾气中n(NO2) :n(NO)=1:1时,过量的NaOH溶液能将氮氧化物全部吸收,只生成一种钠盐,化学方程式为__________。若用步驟④后含硫酸的母液来吸牧氮氧化物,其优点是_____,缺点是________。
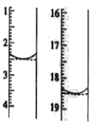
(7)二水合草酸晶体纯度的测定。称取该晶体0.12g,加水溶解,用0.020 mol L-1的酸性KMnO4溶液滴定(杂质不参与反应),该反应的离子方程式为 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2+8H2O。此时溶液颜色由_____变为_____。滴定前后液面读数如图所示,则该晶体中二水合草酸的质量分数为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒容密闭容器中存在下列平衡:CO(g)+H2O(g)![]() CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如右图所示。下列说法错误的是
CO2(g)+H2(g)。CO2(g)的平衡物质的量浓度c(CO2)与温度T的关系如右图所示。下列说法错误的是

A. 在T2时,若反应进行到状态D,则一定有v正<v逆
B. 平衡状态A与C相比,平衡状态A的c(CO)小
C. 若T1、T2时的平衡常数分别为K1、K2,则K1<K2
D. 反应CO(g)+H2O(g)![]() CO2(g)+H2(g)的△H>0
CO2(g)+H2(g)的△H>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com