
����Ŀ����1���л���A�ĺ������ͼ���£�

A�Ľṹ��ʽΪ________________��
��2���л���Bֻ��C��H��O����Ԫ�أ������ģ����ͼ��ʾ![]() �������й���12��ԭ�ӣ�ͼ��������֮������ߴ���������˫���Ȼ�ѧ�����������ʵĽṹ��ʽΪ___________��
�������й���12��ԭ�ӣ�ͼ��������֮������ߴ���������˫���Ȼ�ѧ�����������ʵĽṹ��ʽΪ___________��
��3������ʽ![]() ��ʾ���л���C�ķ���ʽΪ_____________________________��
��ʾ���л���C�ķ���ʽΪ_____________________________��
��4��![]() �к��еĹ����ŵ�����Ϊ___________________________________��
�к��еĹ����ŵ�����Ϊ___________________________________��
��5����ϵͳ�������������л���CH3CH��C2H5��CH��CH3��2��������_________________��
��6��д�����и��л���Ľṹ��ʽ��
��֧��ֻ��һ���һ�����Է���������С������_______________________________��
��2��3������1����ϩ_______________________________________________________��
���𰸡� CH3CH2OCH2CH3 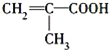 C6H14 �ǻ������� 2��3�������� CH��C2H5��3 CH2�TC��CH3��CH��CH3��2
C6H14 �ǻ������� 2��3�������� CH��C2H5��3 CH2�TC��CH3��CH��CH3��2
����������1�������л���A�ĺ������ͼ��֪�����к����Ѽ����ԳƵ��һ�������A�Ľṹ��ʽΪCH3CH2OCH2CH3����2���л���Bֻ��C��H��O����Ԫ�أ�����B�ķ���ģ�Ϳ��жϷ����к��м����Ȼ���̼̼˫������˸����ʵĽṹ��ʽΪ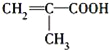 ����3������ʽ
����3������ʽ![]() ��ʾ���л���C��2�������飬����ʽΪ C6H14����4��
��ʾ���л���C��2�������飬����ʽΪ C6H14����4��![]() �к��еĹ����ŵ�����Ϊ���ǻ�����������5���л���CH3CH(C2H5)CH(CH3)2����������ϵͳ��������������������2��3������������6����֧��ֻ��һ���һ�����Է���������С��������������������5��̼ԭ�ӣ��ṹ��ʽΪCH(C2H5)3����2��3������1����ϩ�Ľṹ��ʽΪCH2��C(CH3)CH(CH3)2��
�к��еĹ����ŵ�����Ϊ���ǻ�����������5���л���CH3CH(C2H5)CH(CH3)2����������ϵͳ��������������������2��3������������6����֧��ֻ��һ���һ�����Է���������С��������������������5��̼ԭ�ӣ��ṹ��ʽΪCH(C2H5)3����2��3������1����ϩ�Ľṹ��ʽΪCH2��C(CH3)CH(CH3)2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������к͵ζ�ʱ����Ҫ����ʢ��Һ��ϴ�������ǣ���������ˮϴ����
A.��ʽ�ζ���B.�ձ�
C.��ƿD.��Ͳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͭ��һ������Ũ���ᷴӦ���õ�����ͭ��Һ��NO��NO2�Ļ������4.48L(��״̬)����Щ������һ�����O2����״������Ϻ�ͨ��ˮ�У�����������ȫ��ˮ�����������ᡣ������������ͭ��Һ�м���5mol/LNaOH��Һ��Cu2+ǡ����ȫ����������NaOH��Һ�������60mL������˵���������( )
A. ��������к�NO1.12L B. �μӷ�Ӧ��������0.5mol
C. ��������1.68L D. �˷�Ӧ������ת��0.6mol�ĵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�˵����ȷ����( )
A��ʵ������������Ϊ�˼ӿ췴Ӧ���ʣ�����ϡ H2SO4 �еμ����� Cu(NO3)2 ��Һ
B��N2(g)+3H2(g) ![]() 2NH3(g) ��H��0���������¶ȣ���ƽ��ʱ����ת��������
2NH3(g) ��H��0���������¶ȣ���ƽ��ʱ����ת��������
C�����ȷ�Ӧ��TiO2(s)+2Cl2(g) =TiCl4(g)+O2(g)��һ�������¿��Է����У���÷�Ӧ��S��0
D����ϡAgNO3��Һ�м������ NaCl��Һ��������ɫ�������ټ������� Na2S��Һ�����ֺ�ɫ������������Na2S��Һ�� c(Ag+) ��С��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2017��5��5���й���ɻ�C919�ɹ��ɣ��������ҹ���һ�����������ϵ����ߴ�ɻ��������죡�ɻ��������Ҫ����Ϊ����þ�ȣ������м�������ͭ���ɻ��������Ĺؼ���λ�IJ�����̼���ٵȡ��ش��������⣺
��1��ͭԪ�ص���ɫ��Ӧ����ɫ��������ɫ���Ӧ�ķ��䲨��Ϊ____________(����ĸ)nm��
A. 404 B.543 C. 663 D. 765
��2����̬Cuԭ���У��������ռ�����{�ܲ�ķ�����_______��ռ�ݸ��ܲ���ӵĵ���������ͼ��״Ϊ___________����Ԫ�غ�ͭԪ������ͬһ���ڣ��Һ����������ӹ�����ͬ���������ص��۵㡢�е㶼�Ƚ���ͭ�ͣ�ԭ����_________________________________��
��3���ִ��ɻ�Ϊ�˼�����������������dz�ѹ������ͨ�����ø��ϲ��ϡ���������ά��ǿ���ϣ���ɷ�֮һΪ������֬��������E51�ͻ�����֬�в��ֽṹ��ͼa��ʾ������̼ԭ�ӵ��ӻ���ʽΪ______��


��4��ͼbΪ̼���پ����һ���ֽṹ��̼ԭ��Ƕ������ٵľ���ļ�϶�������ƻ�ԭ�н����ľ����γ���϶�����壬Ҳ��Ϊ��϶������ڴ˽ṹ�У�1����ԭ����Χ������ԭ�������̼ԭ����__________�����þ���Ļ�ѧʽΪ_________________��
��5���ò��־�������ΪVcm3����̼���ٵ��ܶ�Ϊ______________����NA����ʾ����٤��������ֵ��g��cm-3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪Ag2SO4��KWΪ2.0��10-3��������Ag2SO4��������100 mLˮ�����պñ��ͣ��ù�����Ag+��SO42-Ũ����ʱ��仯��ϵ����ͼ������Ag2SO4��Һ��c(Ag+)��0.034 mol��L-1������t1ʱ����������ϵ�м���100 mL. 0.020 mol��L-1Na2SO4��Һ������ʾ��ͼ�У�����ȷ��ʾt1ʱ�̺�Ag+��SO42-Ũ����ʱ��仯��ϵ���ǣ� ��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ݸ�Ŀ������ʯ����һ�����أ�ʯ���ɽ������������˲ɸ���֮����ɹ���ջң���ˮ��֭������������ʯ��ϴ�·��棬��ȥ�����档�������ʯ������ָ
A. KOH B. KAl (SO4)2 C. KHCO3 D. K2CO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£���Ӧ��C(s)��CO2(g)![]() 2CO(g) ��H��0��һ�̶����ܱ������з���������˵����ȷ����
2CO(g) ��H��0��һ�̶����ܱ������з���������˵����ȷ����
A. ���߷�Ӧ�¶ȣ�����Ӧ�������ӣ��淴Ӧ�����½�
B. CO2���������ʺ�CO����������֮��Ϊ1��2ʱ����Ӧ�ﵽ��ѧƽ��״̬
C. �����������ܶ����жϷ�Ӧ�Ƿ�ﵽƽ��
D. 0.2mol��C��0.1mol��CO2��ַ�Ӧ���ɵ�CO�����ʵ���һ��С��0.2mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȡ16.0 mL 10.0 mol��L��1HCl��Һ��������ˮϡ����100 mL��ȡ����ϡ�ͺ��HCl��Һ��25 mL���ֱ�����������Mg��Al����ͬ�����³�ַ�Ӧ�����������������ʱ��仯��������ͼ��ʾ(�������������ɱ�״���µ����)������㣺

��1��ϡ�ͺ�HCl��Һ�����ʵ���Ũ��Ϊ__________mol��L��1��
��2������Mg������������__________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com