
下列各项叙述中,正确的是 ( )
A.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态
B.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素
C.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同
D.24Cr原子的电子排布式是1s22s22p63s23p63d44s2
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
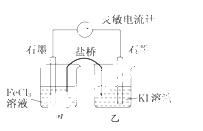 控制适合的条件,将反应2Fe3++2I-
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成
2Fe2++I2设计成 如下图所示的原电池.下列判断不正确的是 ( )
如下图所示的原电池.下列判断不正确的是 ( )
A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中的石墨电极为负极
查看答案和解析>>
科目:高中化学 来源: 题型:
对Na、Mg、Al的有关性质的叙述正确的是 ( )
A.碱性:NaOH<Mg(OH)2<Al(OH)3
B.第一电离能:Na<Mg<Al
C.电负性:Na>Mg>Al
D.还原性: Na>Mg>Al
Na>Mg>Al
查看答案和解析>>
科目:高中化学 来源: 题型:
甲~辛等元素在周期表中的相对位置如下表。甲和戊的原子序数相差3,
戊的一种单质是自然界硬度最大的物质,丁和辛属同周期元素。下列 判断正确的是( )
判断正确的是( )
 A.金属性:甲>乙>丁
A.金属性:甲>乙>丁
B.原子半径:辛>己>戊
C.丙和庚的原子核外电子数相差13
D.乙的单质在空气中燃烧生成只含离子键的化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
W、X、Y、Z四种短周期元素在元素周期表中的相对位置如图所示,W的气态氢化物可
与其最高价含氧酸反应生成离子化合物,由此可知
| W | X | |
| Y | Z |
A.X、Y、Z中最简单氢化物稳定性最弱的是Y
B.Z元素氧化物对应水化物的酸性一定强于Y
C.X元素形成的单核阴离子还原性大于Y
D.Z元素单质在化学反应中只表现氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学用语或模型表示不正确的是
A.中子数为14的硅原子: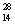 Si
Si
B.CH4分子的比例模型:
C.聚乙烯的结构简式: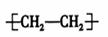
D.次氯酸分子的结构式:H—O-Cl
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于钠元素的几种表达式错误的是 ( )
A.Na+的电子排布图:
B.Na+的结构示意图: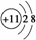
C.Na的电子排布式:1s22s22p63s1
D.Na的简化电子排布式:[Na]3s1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述或操作正确的是 ( )
A.浓硫酸具有强氧化性,稀硫酸无氧化性
B.浓硫酸滴到蓝矾上,蓝矾变成白色粉末,体现了浓硫酸的脱水性
C.稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌
D.浓硫酸与铜的反应中,浓硫酸仅表现强氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com