
【题目】将8.7 g MnO2与足量浓盐酸混合加热,反应生成氯气的体积(标准状况)是多少L?;被氧化的HCl的质量是多少g?。
科目:高中化学 来源: 题型:
【题目】世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色”消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备ClO2的流程如下:

(1) ClO2中所有原子_____________(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用_________
A.饱和食盐水 B.碱石灰 C.浓硫酸 D.蒸馏水
(2) 稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是_________
A.二氧化氯可广泛用于工业和饮用水处理
B.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围
C.在工作区和成品储藏室内,要有通风装置和监测及警报装置
(3) 欧洲国家主要采用氯酸钠氧化浓盐酸制备。化学反应方程式为______________________。
(4) 我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式是 __________________,此法相比欧洲方法的优点是______________________。
(5) 科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学反应方程式为_____________________________。此法提高了生产及储存、运输的安全性,原因是 _________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】五氟化碘(IF5)是重要的卤氟化物,IF5可与水反应IF5+3H2O=HIO3+5HF,生成的HIO3 与KI在酸性下生成游离碘IO3-+5I-+6H+=3I2+3H2O。用标准硫代硫酸钠溶液滴定碘发生反应2Na2S2O3+I2=Na2S4O6+2NaI即可分析IF5含量,若己知滴定耗用硫代硫酸钠的物质的量为0.3mol,则分析的试样中IF5的物质的量为
A. 0.05mol B. 0.2mol C. 0.lmol D. 0.3mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
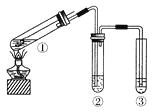
A. 上下移动①中铜丝可控制SO2的量
B. ②中选用品红溶液验证SO2的生成
C. ③中选用NaOH溶液吸收多余的SO2
D. 为确认CuSO4生成,向①中加水,观察颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示各装置设计一个实验,验证浓硫酸与木炭粉在加热条件下反应产生的各种产物。

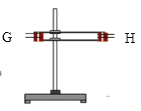
(1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母):
A接G,H接C,D接_______,_______接C,D接B ;
(2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2?乙中_____________________________,丙中_____________________________;
(3)丁中酸性KMnO4溶液的作用是___________________________________________;
(4)写出甲中反应的化学方程式_________________________________________ 。
(5)硫酸有很多的性质,将下列性质对应的字母填入各小题后面对应的括号中:
A.脱水性 B.酸性 C.强氧化性 D.吸水性
Ⅰ.在化学实验中,浓硫酸可做SO2、CO2等气体的干燥剂。 (_______)
Ⅱ.Na2CO3与H2SO4反应,可生成Na2SO4和CO2。 (_______)
Ⅲ.向滤纸上滴加浓H2SO4 ,滤纸变黑。 (_______)
Ⅳ.在冷浓H2SO4中放入铁片没明显现象 (_______)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组用如图装置制取、收集纯净干燥的氨气,并探究氨气的有关性质。

回答下列问题:
(1)开始实验之前要进行的操作是________________________________
(2)写出利用装置I制取氨气的化学方程式_____________________________。
(3)按照a、f、e、b、c、d的顺序将仪器连接,装置Ⅲ中倒置漏斗的作用是____________,装置IV中仪器的名称为_____________,盛装的试剂为_____________。
(4)向NH3的水溶液中滴加1~2滴酚酞溶液,溶液颜色由无色变________色,说明溶液显____性,写出其电离方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验或操作方法正确的是
A. 用蘸有待测液的铁丝,检验K+ 
B. 从食盐水中提取氯化钠
C. 验证NaHCO3和Na2CO3的热稳定性 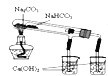
D. 分离水与乙醇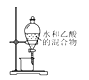
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硝酸钠(NaNO2)是一种重要的工业盐,也常用于鱼类、肉类等食品的染色和防腐,易溶于水,微溶于乙醇. 某化学兴趣小组对亚硝酸钠进行多角度探究:
i.亚硝酸钠的制备
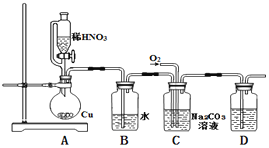
(1)实验中用恒压滴液漏斗,相比普通分液漏斗,显著的优点是____.
(2)D中澄清石灰水变浑浊,则C中制备NaNO2的离子方程式为_______________。
ii. 探究亚硝酸钠与硫酸反应气体产物成分.
已知:①NO+NO2+2OH﹣═2NO2﹣+H2O ②气体液化的温度:NO2:21℃,NO:﹣152℃

(3)反应前应打开弹簧夹,先通入一段时间氮气,目的是___________.
(4)为了检验装置A中生成的气体产物,仪器的连接顺序(按左→右连接):
A、C、______、______、______.
(5)在关闭弹簧夹,打开分液漏斗活塞,滴入70%硫酸后,A中产生红棕色气体.
①确认A中产生的气体含有NO,依据的现象是_________________.
②装置B的作用是____________________.
iii. 设计实验证明酸性条件下NaNO2具有氧化性:___________。
供选用的试剂:NaNO2溶液、KMnO4溶液、FeSO4溶液、KI溶液、稀硫酸、淀粉溶液、KSCN溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水中的溶解氧是水生生物生存不可缺少的条件,某课外小组采用碘量法测定学校周边河水中的溶解氧,实验步骤及测定原理如下:
Ⅰ.取样、氧的固定
用溶解氧瓶采集水样,记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI)混合,反应生成MnO(OH)2,实现氧的固定。
Ⅱ.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I还原为Mn2+,在暗处静置5 min,然后用标准Na2S2O3溶液滴定生成的I2(2![]() +I2=2I+
+I2=2I+![]() )。
)。
回答下列问题:
(1)氧的固定”中发生反应的化学方程式为_________________________________。
(2)Na2S2O3溶液不稳定,使用前需标定。配制该溶液时需要的玻璃仪器有烧杯、胶头滴管、试剂瓶和_________________________,配制溶液定容时俯视会导致Na2S2O3溶液的浓度__________,(填“偏高”或“偏低”)蒸馏水必须经过煮沸、冷却后才能使用,其目的是杀菌、除________________及二氧化碳。
(3)取100.00 mL水样经固氧、酸化后,用0.5 mol·L1Na2S2O3溶液滴定,以_________作指示剂,如何判断该反应到达终点_________________________________________________;若反应中消耗Na2S2O3溶液的体积为10 mL,则水样中溶解氧的含量为_________mg·L1。
(4)上述滴定完成时,若滴定前平视,滴定后仰视会导致测量结果___________。(填“偏高”或“偏低”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com