
短周期元素A、B、C、D、E的原子序数依次增大,A元素阳离子的原子核外没有电子,B是空气中含量最多的元素;C元素原子最外层电子数是其电子层数的三倍;C与D可形成两种常见的离子化合物;工业上常用电解C与E的化合物来制备E单质。
(1)C、D、E的简单离子半径由小到大的顺序 (用离子符号表示)。
(2)工业上常用A和B的单质合成一种常见气体,该气体的电子式 。检验该气体的常用方法是 。
(3)D2C2与H2O反应的化学方程式是 ,D2C2与CuSO4溶液反应的现象是 。(4)A、B、C三种元素可组成一种常见离子化合物,其水溶液呈酸性,该溶液中离子浓度由大到小的顺序是 。
(5)电动汽车的某种燃料电池,通常用NaOH作电解质,用E单质、石墨作电极,在石墨电极一侧通入空气,该电池的负极反应: 。
每空2分,共14分
(1)Al3+ < Na+ < O2- 2分
(2)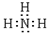 2分,用润湿的红色石蕊试纸接近该气体,若试纸变红,证明氨气存在 2分
2分,用润湿的红色石蕊试纸接近该气体,若试纸变红,证明氨气存在 2分
(3)2Na2O2 + 2H2O = 4NaOH + O2↑ 2分 、产生蓝色沉淀并有气泡放出 2分
(4)CNO3->CNH4+>CH+ >COH- 2分
(5) Al + 4OH- -3e- = AlO2- + 2H2O 2分
【解析】
试题分析:短周期元素A、B、C、D、E的原子序数依次增大, A元素阳离子的原子核外没有电子,则A是H元素;空气中含量最多的是氮气,所以B是N元素;C元素原子最外层电子数是其电子层数的三倍,则C不可能是3层电子,所以C只有两层电子,最外层是6个,所以C是O元素;C与D可形成两种常见的离子化合物,O与Na能形成氧化钠与过氧化钠两种离子化合物,所以D是Na元素;工业上常用电解C与E的化合物来制备E单质,说明电解氧化物得到E单质,则E是Al元素,电解氧化铝得到Al。
(1)根据离子半径的比较,电子层结构相同的离子,随核电荷数的增加,离子半径逐渐减小,所以C、D、E的简单离子半径由小到大的顺序Al3+ < Na+ < O2-;
(2)工业上用氢气和氮气合成氨气,氨气是共价化合物,电子式为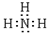 ;检验氨气的方法是用润湿的红色石蕊试纸接近该气体,若试纸变红,证明氨气存在;
;检验氨气的方法是用润湿的红色石蕊试纸接近该气体,若试纸变红,证明氨气存在;
(3)过氧化钠与水反应生成氢氧化钠和氧气,化学方程式是2Na2O2 + 2H2O = 4NaOH + O2↑;所以过氧化钠与硫酸铜溶液反应时,过氧化钠与水反应生成的氢氧化钠与硫酸铜反应生成氢氧化铜的蓝色沉淀,所以D2C2与CuSO4溶液反应的现象是产生蓝色沉淀并有气泡放出;
(4)A、B、C三种元素可组成一种常见离子化合物是硝酸铵,其水溶液呈酸性,是因为铵根离子的水解的作用,硝酸根离子的浓度最大,其次是铵根离子,因为溶液呈酸性,所以氢氧根离子浓度最小,所以溶液中离子浓度的大小顺序是CNO3->CNH4+>CH+ >COH-;
(5)Al-空气电池中,Al与氢氧化钠溶液反应,所以Al作负极,失去电子与氢氧根离子结合为偏铝酸根离子和水,发生的电极反应式为Al + 4OH- -3e- = AlO2- + 2H2O。
考点:考查元素的推断,元素及其化合物的性质判断


科目:高中化学 来源:2014-2015学年福建省高二上学期期中化学(文)试卷(解析版) 题型:选择题
为改善空气质量而启动的“蓝天工程”得到了全民的支持。下列措施不利于“蓝天工程”实施的是
A.推广使用燃煤脱硫技术,减少SO2污染
B.实施绿化工程,防治扬尘污染
C.加快清洁能源的开发利用
D.加大石油、煤炭的开发速度,提倡使用化石燃料
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省高三第一次月考化学试卷(解析版) 题型:选择题
关于下列说法:①Fe(OH) 3胶体和CuSO4溶液都是混合物;②蔗糖、硫酸钡和水分别属于非电解质、强电解质和弱电解质;③冰醋酸、纯碱、小苏打分别属于酸、碱、盐;④、天然气、水煤气和太阳能分别属于化石能源、不可再生能源和新能源;⑤Mg、Al、Cu可以分别用置换法、直接加热法和电解法冶炼得到。其中正确的是
A.①②④ B.①②⑤ C.②③④ D.③④⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省济宁市高三上学期期中化学试卷(解析版) 题型:选择题
化学已经渗透到人类生活的各个方面,下列说法正确的是
A.高纯度的硅单质广泛用于制作光导纤维,光导纤维遇强碱会“断路”
B.氮的固定只有在高温、高压、催化剂的条件下才能实现
C.服用铬含量超标的药用胶囊会对人体健康不会造成危害
D.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,既能杀菌消毒又能净水
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三12月月考化学试卷(解析版) 题型:选择题
在“石蜡→液体石蜡→石蜡蒸气→裂化气”的变化过程中,被破坏的作用力依次是
A.范德华力、范德华力、共价键
B.范德华力、范德华力、范德华力
C.范德华力、共价键、共价键
D.共价键、共价键、共价键
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省高三12月月考化学试卷(解析版) 题型:选择题
同温同压下,在3支体积不同的试管中分别充满等体积混合的2种气体,它们是:①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中溶质的物质的量浓度分别为c1、c2、c3(假设溶质全在试管中),则下列关系正确的是
A.c1>c2>c3 B.c1>c3>c2
C.c1=c3>c2 D.c1=c2>c3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年河北省保定市高三12月联考化学试卷(解析版) 题型:选择题
下列变化过程放热的是
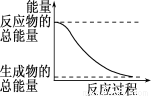
A.H2O(l)→H2O(g)
B.2HI(g)→H2(g)+I2(g)+Q Q=—14.9 kJ/mol
C.形成化学键时共放出能量862 kJ的化学反应
D.能量变化如上图所示的化学反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高二上学期期中化学试卷(解析版) 题型:填空题
氮氧化物是造成雾霾天气的主要原因之一,消除氮氧化物有多种方法。
(1)利用ClO2氧化氮氧化物反应过程如下:
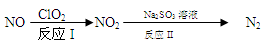
反应I的方程式是2NO+ClO2+H2O == NO2+HNO3+HCl,该反应的氧化产物为 ,
反应II的化学方程式为 。
(2)可用甲烷催化还原氮氧化物。已知:
CH4(g) + 4NO2(g) === 4 NO(g) + CO2(g) + 2H2O(g) ΔH1
CH4(g) + 4NO(g) === 2 N2(g) + CO2(g) + 2H2O(g) ΔH2
①已知NO气体会分解为NO2气体和N2气体,写出该反应的热化学方程式 。
②现有一份NO与NO2的混合气体,其平均相对分子量为34,用16g甲烷气体催化还原该混合气 体,恰好完全反应生成氮气,二氧化碳气体和水蒸气,共放出热量1042.8kJ。则该混合气体中NO和NO2的物质的量之比为 ,若已知上述反应ΔH2= —1160 kJ·mol-1,则ΔH1= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com