
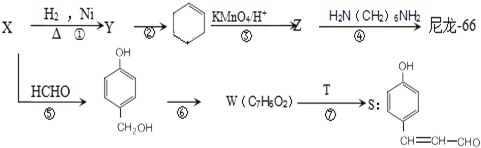
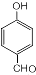
 ,S的分子式为C9H8O2.
,S的分子式为C9H8O2.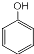 +HCHO$\stackrel{△}{→}$
+HCHO$\stackrel{△}{→}$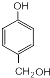 .
.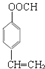 .
. 分析 根据题目中各物转化关系,X与甲醛发生信息Ⅲ的反应生成 ,可推知X为
,可推知X为 ,根据W的分子式与
,根据W的分子式与 比较,可知
比较,可知 发生氧化反应得W为
发生氧化反应得W为 ,
, 与乙醛发生信息Ⅲ的反应生成
与乙醛发生信息Ⅲ的反应生成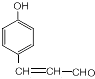 ,所以T为CH3CHO,X与氢气发生加成反应得Y为
,所以T为CH3CHO,X与氢气发生加成反应得Y为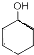 ,Y发生消去反应得环已稀,环已稀被氧化得Z,Z的化学式为C6H10O4,所以Z为HOOHCH2CH2CH2CH2COOH,Z与
,Y发生消去反应得环已稀,环已稀被氧化得Z,Z的化学式为C6H10O4,所以Z为HOOHCH2CH2CH2CH2COOH,Z与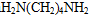 发生缩聚反应生成为尼龙-66为
发生缩聚反应生成为尼龙-66为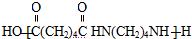 ,据此答题.
,据此答题.
解答 解:根据题目中各物转化关系,X与甲醛发生信息Ⅲ的反应生成 ,可推知X为
,可推知X为 ,根据W的分子式与
,根据W的分子式与 比较,可知
比较,可知 发生氧化反应得W为
发生氧化反应得W为 ,
, 与乙醛发生信息Ⅲ的反应生成
与乙醛发生信息Ⅲ的反应生成 ,所以T为CH3CHO,X与氢气发生加成反应得Y为
,所以T为CH3CHO,X与氢气发生加成反应得Y为 ,Y发生消去反应得环已稀,环已稀被氧化得Z,Z的化学式为C6H10O4,所以Z为HOOHCH2CH2CH2CH2COOH,Z与
,Y发生消去反应得环已稀,环已稀被氧化得Z,Z的化学式为C6H10O4,所以Z为HOOHCH2CH2CH2CH2COOH,Z与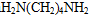 发生缩聚反应生成为尼龙-66为
发生缩聚反应生成为尼龙-66为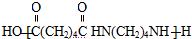 ,
,
(1)根据上面的分析可知,X为 ,X的化学名称为苯酚,W的结构简式为
,X的化学名称为苯酚,W的结构简式为 ,根据S的结构简式可知S的分子式为C9H8O2,
,根据S的结构简式可知S的分子式为C9H8O2,
故答案为:苯酚; ;C9H8O2;
;C9H8O2;
(2)反应②为醇的消去反应,反应的条件为浓硫酸,加热,故答案为:浓硫酸,加热;
(3)据分析属于加成反应的有①⑤,故答案为:①⑤;
(4)反应⑤的化学方程式为 +HCHO$\stackrel{△}{→}$
+HCHO$\stackrel{△}{→}$ ,
,
故答案为: +HCHO$\stackrel{△}{→}$
+HCHO$\stackrel{△}{→}$ ;
;
(5)据S的结构简式可知,S除苯环外还有2个O原子,3个C原子,苯环外有2个不饱和键,其同分异构体①单环芳香族化合物; ②既能发生银镜反应,又能发生水解反应,说明含有甲酸形成的酯基,若只有1个取代基,可以是-CH=CHOOCH,或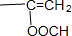 ,若有2个取代基,分别是-CH=CH2,和-OOCH,临间对3种,共5种,苯环上核磁共振氢谱上有2个峰的结构简式为
,若有2个取代基,分别是-CH=CH2,和-OOCH,临间对3种,共5种,苯环上核磁共振氢谱上有2个峰的结构简式为 ,故答案为:5;
,故答案为:5; .
.
点评 该题考查有机物的合成和推断,注意有机物的性质,本题难度中等,可以用逆推和正推相结合的方法,注意有机基础知识的灵活运用.


 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在2L水中溶有80克的NaOH | B. | 80克NaOH溶于2L水配成的溶液 | ||
| C. | 每升溶液中含有80克NaOH | D. | 每2L溶液中含有80克NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | FeCl2溶液(FeCl3):Fe粉 | B. | CO2(SO2):饱和的Na2CO3溶液 | ||
| C. | SO2(HCl):NaOH溶液 | D. | NaHCO3溶液(Na2CO3):Ca(OH)2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
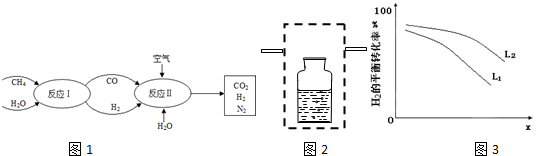
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 “黑索金”是一种烈性炸药.“黑索金”是由乌洛托品(分子结构如图)与发烟硝酸作用制得.下列说法中不正确的是( )
“黑索金”是一种烈性炸药.“黑索金”是由乌洛托品(分子结构如图)与发烟硝酸作用制得.下列说法中不正确的是( )| A. | 乌洛托品中碳原子均达到饱和结构 | |
| B. | 乌洛托品的一氯代物只有一种 | |
| C. | 乌洛托品的分子式为C6H12N4 | |
| D. | 乌洛托品分子结构中含有3个六元环 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电能是一级能源 | B. | 水煤气是二级能源 | ||
| C. | 天然气是二级能源 | D. | 水能是二级能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

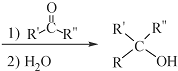
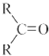 $\stackrel{(C_{6}H_{5})_{3}P=CH_{2}}{→}$
$\stackrel{(C_{6}H_{5})_{3}P=CH_{2}}{→}$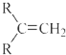 (R表示烃基,R′和R″表示烃基或氢)
(R表示烃基,R′和R″表示烃基或氢)  .写出A中含氧官能团的名称:羟基
.写出A中含氧官能团的名称:羟基 或
或 .(不考虑环状结构)
.(不考虑环状结构) .
.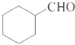 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CHOH.
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2$\stackrel{HBr}{→}$CH3CH2Br$→_{△}^{NaOH溶液}$CH3CHOH.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com