
| A. | 甲烷的球棍模型为 | B. | 乙醇的分子式为C2H3CH2OH | ||
| C. | 邻甲基苯酚的结构简式为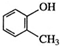 | D. | 聚乙烯的结构简式为CH2=CH2 |
科目:高中化学 来源: 题型:解答题
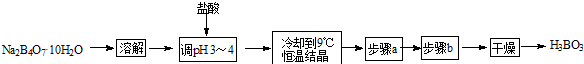


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏 | B. | 水洗后分液 | ||
| C. | 用过量饱和碳酸钠溶液洗涤后分液 | D. | 用过量氢氧化钠溶液洗涤后分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 要提纯的物质 (杂质) | 乙醇 (水) | 乙炔(H2S) | 溴苯 (溴) |
| 选用试剂 | |||
| 分离方法 | 1 |
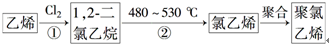
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| I1 | I2 | I3 | I4 | … |
| 496 | 4562 | 6912 | 9540 | … |
| 化学键 | A-A | C≡C | A-C |
| 键能/kJ•mol-1 | 436.0 | 946 | 390.8 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com