
| A. | 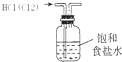 装置可除去HCl中的Cl2杂质 | |
| B. | 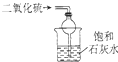 装置可吸收SO2,并防止倒吸 | |
| C. | 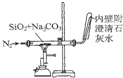 装置石灰水变浑浊即可证明非金属性:Si>C | |
| D. | 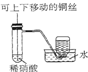 装置可制取并收集NO气体 |
分析 A.HCl极易溶于水,食盐水抑制氯气的溶解;
B.石灰水的浓度小,不利用吸收二氧化硫;
C.装置石灰水变浑浊生成二氧化碳,但不能利用固体之间的反应比较酸性及非金属性;
D.Cu与硝酸反应生成NO,NO不溶于水.
解答 解:A.HCl极易溶于水,食盐水抑制氯气的溶解,则装置吸收HCl,将原物质除去,不能除杂,故A错误;
B.石灰水的浓度小,不利用吸收二氧化硫,应选NaOH溶液吸收,故B错误;
C.装置石灰水变浑浊生成二氧化碳,不能利用二氧化硅与碳酸钠的反应比较酸性及非金属性,事实为非金属性C>Si,故C错误;
D.Cu与硝酸反应生成NO,NO不溶于水,选排水法可收集,则图中装置可制取并收集NO气体,故D正确;
故选D.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、非金属性比较、气体的制备及收集等,把握物质的性质、反应原理及实验装置的作用为解答的关键,侧重分析与实验能力的考查,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 凡是放热反应的发生均无需加热 | |
| B. | 凡是需要加热后才能发生的反应一定是吸热反应 | |
| C. | 伴有能量变化的物质变化都是化学变化 | |
| D. | 物质发生化学反应都伴随着能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X与Y形成化合物时,X可以显负价,Y显正价 | |
| B. | 气态氢化物的稳定性:HmY小于HnX | |
| C. | 第一电离能可能Y小于X | |
| D. | 最高价含氧酸的酸性:X对应的酸的酸性弱于Y对应的酸的酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 泡沫灭火器中用的是苏打和硫酸铝 | |
| B. | 通过干馏可将煤中含有的苯、甲苯等物质分离出来 | |
| C. | 地沟油通过水解反应可得到车用汽油 | |
| D. | 家庭用洁厕灵与“84消毒液”不能同时使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
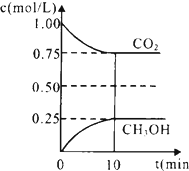 二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.
二氧化碳是引起“温室效应”的主要物质,节能减排,高效利用能源,能够减少二氧化碳的排放.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | A、B、C三种元素形成的化合物一定是非电解质 | |
| B. | A与C只能形成化学式为A2C的化合物 | |
| C. | 第三周期中,D的原子半径最大 | |
| D. | E的氧化物对应的水化物一定具有强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
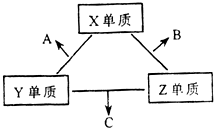 X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化:
X、Y、Z三种短周期元素,它们的原子序数之和为16.X、Y、Z三种元素的常见单质在常温下都是无色气体,在适当条件下可发生如下变化: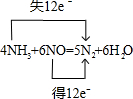
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com