
【题目】已知2H2O2(l)═2H2O(l)+O2(g)反应过程中的能量变化曲线如图所示,下列说法不正确的是( )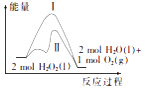
A.该反应的△H<0,△S>0
B.途径Ⅱ与途径I相比,可能是加了催化剂
C.其他条件相同时,产生相同体积的氧气时放出的热量:途径I>途径Ⅱ
D.其他条件相同时,产生相同体积的氧气所需的时间:途径I>途径Ⅱ
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知NaHSO2溶液在不同温度下均可被过量KlO3氧化,当NaHSO3完全消耗即有I2析出,依据I2析出所需时间可以求得NaHSO3的反应速率.将浓度均为0.020 molL﹣1的NaHSO3溶液(含少量淀粉)10.0 mL、KIO3(过量)酸性溶液40.0 mL混合,记录10~55℃间溶液变蓝时间,55℃时未观察到溶液变蓝,实验结果如图.据图分析,下列判断不正确的是( ) 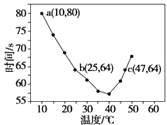
A.40℃之前与40℃之后溶液变蓝的时间随温度的变化趋势相反
B.图中a点对应的NaHSO3反应速率为5.0×10﹣5 molL﹣1s﹣1
C.图中b、c两点对应的NaHSO3反应速率相等
D.40℃之后,淀粉不宜用作该实验的指示剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上一般在恒容密闭容器中采用下列反应合成甲醇:CO(g)+2H2(g)CH3OH(g)
(1)判断反应达到平衡状态的依据是(填字母序号,下同) .
A.生成CH3OH的速率与消耗CO的速率相等
B.混合气体的密度不变
C.混合气体的相对平均分子质量不变
D.CH3OH,CO,H2的浓度都不再发生变化
E.气体的压强不再改变
(2)表所列数据是该反应在不同温度下的化学平衡常数(K).
温度 | 250℃ | 300℃ | 350℃ |
K | 2.041 | 0.270 | 0.012 |
某温度下,将2molCO和6molH2充入2L的密闭容器中,充分反应后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为 , 此时的温度为 .
(3)要提高CO的转化率,可以采取的措施是 .
a.升温 b.加入催化剂 c.增加CO的浓度 d.恒容下加入H2使压强变大
e.恒容下加入惰性气体使压强变大 f.分离出甲醇
(4)在250℃时,测得某密闭容器中各物质的物质的量浓度见表:
CO | H2 | CH3OH |
0.5molL﹣1 | 2molL﹣1 | 6molL﹣1 |
此时反应的正、逆反应速率的关系是:v(正)v(逆)(填“>”“<”或“═”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于燃料充分利用的说法错误的是 ( )
A. 热能要充分利用 B. 充足的空气就是指空气的量越大越好
C. 固体燃料燃烧前要粉碎 D. 液体燃料燃烧时可以雾状喷出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应C(s)+H2O(g)H2(g)+CO(g),△H>0达到平衡后,改变某一外界条件(不改变物质的量的条件下),反应速率v与时间t的关系如图. 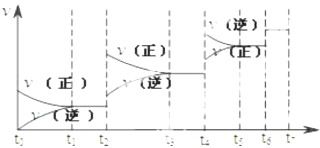
①图中t2到t3段、t4到t6段时引起平衡移动的条件分别可能是、;
②图中表示平衡混合物中CO的含量最高的一段时间是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式为  ,下列说法正确的是( )
,下列说法正确的是( )
A.该物质的分子式为C11H10O3
B.该有机物含有4种官能团
C.1 mol该有机物最多可以消耗2 mol NaOH
D.该有机物不能发生消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按下图装置,持续通入气体X,可看到a处有红色物质生成,b处变蓝,c处得到液体,则气体X可能是( )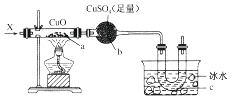
A.H2
B.CO和H2
C.NH3
D.CH3CH2OH(蒸气)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,表中所列的字母分别代表一种化学元素.试回答下列问题: 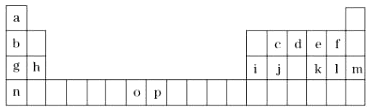
(1)元素o为25号元素,请写出其基态原子的电子排布式 .
(2)d与a反应的产物的分子中,中心原子的杂化形式为 .
(3)d、e、f三种元素的电负性大小顺序为(用元素符号表示) .
(4)o、p两元素的部分电离能数据列于表:
元素 | O | P | |
电离能/KJmol﹣1 | I1 | 717 | 759 |
I2 | 1509 | 1561 | |
I3 | 3248 | 2957 | |
比较两元素的I2、I3可知,气态o2+再失去一个电子比气态p2+再失去一个电子难.对此,你的解释是 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com