
| A. | 标准状况下,22.4L H2O含有NA个分子 | |
| B. | 1L 1mol•L -1的NaClO 溶液中含有ClO-的数目少于NA个 | |
| C. | 0.1molAlCl3完全转化为氢氧化铝胶体,生成0.l NA个胶体粒子 | |
| D. | 0.1molCl2与足量NaOH溶液反应,转移电子数为0.2 NA |
分析 A、标况下水为液态;
B、次氯酸根为弱酸根,在溶液中会水解;
C、一个氢氧化铝胶粒是多个氢氧化铝的聚集体;
D、氯气和碱的反应为歧化反应.
解答 解:A.在标准状况下H2O是液态,不能使用气体摩尔体积来计算其物质的量和分子个数,故A错误;
B.由于NaClO 是强碱弱酸盐,弱酸根离子会发生水解反应而消耗,所以在1L 1mol•L -1的NaClO 溶液中含有ClO-的数目少于NA个,故B正确;
C.胶体粒子是许多氢氧化铁聚集的颗粒,故生成的胶体粒子小于0.l NA,故C错误;
D.氯气和碱的反应为歧化反应,1mol氯气转移1mol电子,故0.1molCl2与足量NaOH溶液反应,转移电子数为0.1 NA,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 优等生题库系列答案
优等生题库系列答案科目:高中化学 来源: 题型:多选题
| A. | 1:1 | B. | 1:2 | C. | 3:1 | D. | 1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(CH3COOH)+2c(H+)=c(CH3COO-)+2c(OH-) | B. | c(HAc)>c(CH3COO-) | ||
| C. | 2c(H+)=c(CH3COO-)-c(CH3COOH) | D. | c(CH3COOH)+c(CH3COO-)=0.02mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
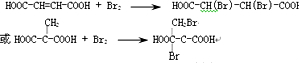
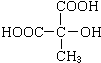 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
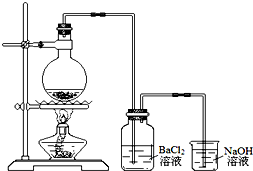 某学习小组探究铜跟浓硫酸反应的情况.取6.4g铜片和10mL 18mol•L-1的浓硫酸放在圆底烧瓶中,按如图所示装置进行实验.
某学习小组探究铜跟浓硫酸反应的情况.取6.4g铜片和10mL 18mol•L-1的浓硫酸放在圆底烧瓶中,按如图所示装置进行实验.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2、Br2、I2 | B. | Br2、Cl2、I2 | C. | I2、Cl2、Br2 | D. | I2、Br2、Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C生成的速率与C分解的速率不相等 | |
| B. | A、B、C的浓度不再变化 | |
| C. | 单位时间生成nmolA,同时生成3nmolB | |
| D. | A、B、C的分子数之比为1:3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
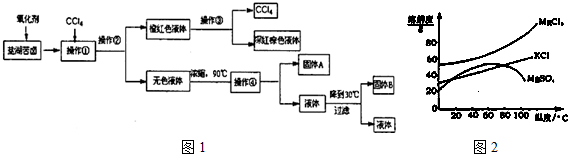
| 化学式 | BaCO3 | BaSO4 | Ca(OH)2 | MgCO3 | Mg(OH)2 |
| Ksp | 8.1×10一9 | 1.08×10一10 | 1.0×10一4 | 3.5×10一5 | 1.6×10一11 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com