
(19��)��1����֪��1 mol H��H����1 mol I��I��1 mol H��I���ֱ���Ҫ���յ�����Ϊ436 kJ��151 kJ��299 kJ,���������͵ⷴӦ����1 mol HI��Ҫ ����ų��������ա��� kJ��������
��2����֪�ڳ��³�ѹ�£�
��CH3OH��l��+O2��g��=CO��g��+2H2O��l������H1=��442.8 kJ��mol
��2CO(g)+O2(g)��2CO2(g)����H2 ����566.0 kJ��mol
д����ʾ�״�ȼ���ȵ��Ȼ�ѧ����ʽ__________________________________________
��3����֪�ϳɰ����Ȼ�ѧ����ʽΪ��N2(g)+3H2(g) 2NH3(g)����H= -92.2 kJ��mol��1
2NH3(g)����H= -92.2 kJ��mol��1
�±��Ǻϳɰ���Ӧ��ij�¶���2.0L���ܱ������н���ʱ����õ����ݣ�
���ʵ�����mol�� | 0 | 1 | 2 | 3 | 4 |
N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
���ݱ������ݼ��㣺
�ٷ�Ӧ���е�2Сʱʱ�ų�������Ϊ kJ��
��0~1Сʱ��N2��ƽ����Ӧ���� mol��L��1��h��1
�۴������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K= (������λС��)��
�ܷ�Ӧ�ﵽƽ�������ƽ����ϵ���ټ���N2��H2��NH3��1mol����ѧƽ���� �����ƶ��������Ӧ�����淴Ӧ�����ƶ�����
��1���ų� �� 5.5��ÿ��2�֣�
��2��CH3OH��l��+ 3/2O2��g��=CO2��g��+2H2O��l������H=-725.8 kJ/mol
��3���� 27.66 ��0.05 ��0.15 ������Ӧ��ÿ��3�֣�
��������
�����������1����Ӧ�жϿ�1 mol H��H����1 mol I��I��Ҫ���յ�����Ϊ436+151=587kJ���γ�2Ħ�������ͷŵ�����Ϊ299��2=598kJ,���Էų��ı����յĶ࣬��ӦΪ�ų�������ÿ����2Ħ���⻯�⣬�ų�������Ϊ598-587=11kJ����������1Ħ���⻯��ų�5.5kJ����������2�����ݸ�˹���ɣ���+�ڡ�2�����Ȼ�ѧ����ʽΪ��CH3OH��l��+ 3/2O2��g��=CO2��g��+2H2O��l������H=-725.8 kJ/mol����3���ٽ��е�2Сʱ��������Ӧ��1.50-1.20=0.3Ħ�����ʷ�Ӧ����Ϊ0.3��92.2=27.66kJ���ڷ�Ӧ1Сʱ��������Ӧ��4.50-4.20=0.30Ħ����������Ӧ��0.10Ħ�������Ե�����ƽ������=0.10��2��1=0.05 mol��L��1��h��1����ƽ��ʱ������Ũ��Ϊ0.5mol/L��������Ũ��Ϊ0.5 mol/L��������Ũ��Ϊ1.5 mol/L����ƽ�ⳣ��=(0.5)2/[0.5��(1.5)3]=0.15���ܣ����ٶ�����1Ħ��ʱ������Ũ����=12/1��23=0.125<0.15������ƽ�������ƶ���
���㣺��Ӧ�ȵļ��㣬��˹���ɣ�ƽ�ⳣ���ļ��㣬����Ũ���̺�ƽ�ⳣ���ж��ƶ�����


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�����и߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ������
��13�֣����ݻ�Ϊ1��00L�������У�ͨ��һ������N2O4��������ӦN2O4(g) 2NO2(g)�����¶����ߣ�����������ɫ���
2NO2(g)�����¶����ߣ�����������ɫ���
�ش��������⣺
��1����Ӧ�ġ�H 0������ڡ���С�ڡ�����100��ʱ����ϵ�и�����Ũ����ʱ��仯��ͼ��ʾ����0~60sʱ�Σ���Ӧ����v(N2O4)Ϊ mol?L-1?s-1��Ӧ��ƽ�ⳣ��K1Ϊ ��
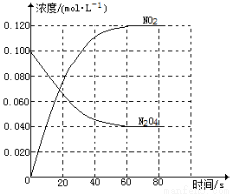
��2��100��ʱ�ﵽƽ��ı䷴Ӧ�¶�ΪT��c(N2O4)��0��0020 mol?L-1?s-1��ƽ�����ʽ��ͣ���10s�ִﵽƽ�⡣
��T 100�棨����ڡ���С�ڡ������ж������� ��
����ʽ�����¶�Tʱ��Ӧ��ƽ�ⳣ��K2 ��
��3���¶�Tʱ��Ӧ��ƽ�����Ӧ�������ݻ�����һ�룬ƽ���� ________�������Ӧ�����淴Ӧ���������ƶ����ж������� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪299 Kʱ���ϳɰ���Ӧ N2 (g ) + 3H2 ( g ) 2NH3 ( g ) ��H = -92.0 kJ/mol�������¶��µ�1 mol N2 ��3 mol H2 ����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������Ϊ������������ʧ��
2NH3 ( g ) ��H = -92.0 kJ/mol�������¶��µ�1 mol N2 ��3 mol H2 ����һ�ܱ������У��ڴ�������ʱ���з�Ӧ����÷�Ӧ�ų�������Ϊ������������ʧ��
A.һ������92.0 kJ B.һ������92.0 kJ
C.һ��С��92.0 kJ D.����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ�У���ȷ����
A��̼��������Һ��ϡ�����ϣ�HCO3-��H��===H2O��CO2��
B��ϡ���������Ƭ�ϣ� 2Fe��6H��===2Fe3����3H2��
C������ͭ��Һ������������Һ��ϣ�CuSO4��2OH��===Cu(OH)2����SO42��
D����������Һ���Ȼ�����Һ��ϣ�AgNO3��Cl��===AgCl����NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ������ʡ��һ��ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���и��������У�������������ͬ����
A��10 g H2��10 g O2 B��5.6 L N2(��״��)��44 g CO2
C��9 g H2O��0.5 mol Br2 D��224 mL H2(��״��)��0.1 mol N2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡУ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪����ʱ��0.1mo1/LijһԪ��HA��ˮ����0.1���������룬���������������
A������Һ��c(H+) = 10-4 mol/L
B�������¶ȣ���Һ��pH����
C������ĵ���ƽ�ⳣ��ԼΪ1��10-7
D��������Һ��ˮϡ�ͺ����HA����������0.1%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ��ɽ��ʡУ�߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
��ƽ����ƿ�з�����������������Ȼ�茶��壬����ƿ������ľ���ϵ�����ˮ��һ����ͻᷢ��ƿ�ڹ�̬���ʱ��Һ�壬ƿ�ڱ��䣬Сľ����������ˮ���ᣬ������ƿճס����ʱ��ƿ���������������а�ζ�������Է��ط����˷�ӦBa(OH)2��8H20(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)���н�������ȷ����
A���Է���Ӧһ���Ƿ��ȷ� B���Է���Ӧһ�������ȷ�Ӧ
C���е����ȷ�ӦҲ���Է����� D�����ȷ�Ӧ�����Է�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015ѧ�����ʡ�����и�һ12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij��Һ�к���HCO3����Na����Ba2����NO3�� 4�����ӣ��������м�������Na2O2�������Һ������Ũ�Ȼ������ֲ������
A��HCO3�� B��Na�� C��Ba2�� D��NO3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ����и߶���ѧ�ڵ�����������⻯ѧ�Ծ��������棩 ���ͣ������
��12�֣�
��1��������������ʵ���Ũ�ȵĴ��������������Һ��Ϻ���Һ�� ������ԡ��������ԡ����ԡ�����ͬ������Һ��c(Na��) c(CH3COO��)��� >�� ������<�� ����
��2��pH��3�Ĵ����pH��11������������Һ�������Ϻ���Һ�� ����Һ��c(Na��) c(CH3COO��)��
��3�����ʵ���Ũ����ͬ�Ĵ��������������Һ��Ϻ���Һ�д�������Ӻ�������Ũ����ȣ����Ϻ���Һ�� ��������� ����������Һ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com