
(16分)硫代硫酸钠是一种重要的化工产品。某兴趣小组拟制备硫代硫酸钠晶体(Na2S2O3·5H2O)。
I.【查阅资料】
(1)Na2S2O3·5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成。
(2)向Na2CO3和Na2S混合溶液中通入SO2可制得Na2S2O3;所得产品常含有少量Na2SO3和Na2SO4。
(3)Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl。
II.【制备产品】
实验装置如图所示(省略夹持装置):
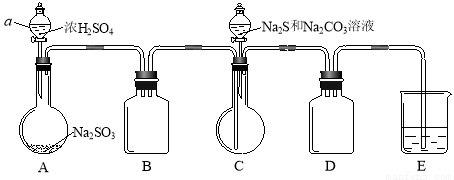
实验步骤:
(1)检查装置气密性,按图示加入试剂。
仪器a的名称是 ;E中的试剂是 (选填下列字母编号)。
A.稀H2SO4 B.NaOH溶液 C.饱和NaHSO3溶液
(2)先向C中烧瓶加入Na2S和Na2CO3混合溶液,再向A中烧瓶滴加H2SO4。
(3)等Na2S和Na2CO3完全消耗后,结束反应。过滤C中混合物,滤液 (填写操作名称)、结晶、过滤、洗涤、干燥,得到产品。
III.【探究与反思】
(1)为验证产品中含有Na2SO3和Na2SO4,该小组设计了以下实验方案,请将方案补充完整。(所需试剂从稀HNO3、稀H2SO4、稀HCl、蒸馏水中选择)
取适量产品配成稀溶液,
,则可确定产品中含有Na2SO3和Na2SO4。
(2)为减少装置C中生成Na2SO4的量,在不改变原有装置的基础上对实验步骤(2)进行了改进,改进后的操作是
。
(3)Na2S2O3·5H2O的溶液度随温度升高显著增大,所得产品通过 方法提纯。
(4)利用黄铜矿冶炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3)可制备Fe2O3。方法为:
①用稀盐酸浸取炉渣,过滤。
②滤液先氧化,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得Fe2O3。
a.除去Al3+的离子方程式是 。
b.选用提供的试剂,设计实验验证炉渣中含有FeO。
提供的试剂:稀盐酸、稀硫酸、KSCN溶液、KMnO4溶液、NaOH溶液、碘水
所选试剂为 。
(每空2分)
II (1)分液漏斗 B (3)蒸发
III (1)取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀HCl,若沉淀未完全溶解,并有刺激性气味的气体产生,
(2)先向A中烧瓶滴加浓H2SO4,产生的气体将装置中空气排尽后,再向C中烧瓶加入Na2S和Na2CO3混合溶液。
(3)重结晶
(4)a:Al3++4OH—=AlO2—+2H2O;(2分)
b:稀硫酸、KMnO4溶液;(2分,各1分)
【解析】
试题分析:II(1)仪器a的名称是分液漏斗;E中的试剂是NaOH溶液,目的是吸收剩余的二氧化硫,因为二氧化硫能与氢氧化钠溶液反应,与稀H2SO4和饱和NaHSO3溶液不反应,故答案为: B。
(3)将Na2S2O3结晶析出的操作应为:蒸发、结晶、过滤、洗涤、干燥。
Ⅲ.【探究与反思】
(1)根据:Na2S2O3?5H2O是无色透明晶体,易溶于水,其稀溶液与BaCl2溶液混合无沉淀生成;Na2SO3易被氧化;BaSO3难溶于水,可溶于稀HCl;BaSO4难溶于水,难溶于稀HCl,以及硝酸具有强氧化性、加入硫酸会引入硫酸根离子可知,取适量产品配成稀溶液,滴加足量BaCl2溶液,有白色沉淀生成,过滤,用蒸馏水洗涤沉淀,向沉淀中加入足量稀盐酸,若沉淀未完全溶解,并有刺激性气味的气体产生,则可以确定产品中含有Na2SO3和Na2SO4。
(2)因为亚硫酸钠易被氧化生成硫酸钠,所以为减少装置C中生成Na2SO4的量,改进后的操作是先向A中烧瓶滴加浓硫酸,产生的气体将装置中的空气排尽后,再向C中烧瓶加入硫化钠和碳酸钠的混合溶液。
(3)Na2S2O3?5H2O的溶解度随温度升高显著增大,所得产品通过重结晶方法提纯。
(4)a.氧化铝是两性氧化物,能和强酸以及强碱反应,除去铝离子的反应是利用过量氢氧化钠溶液和铝离子反应生成四羟基合铝,离子方程式为: Al3++4OH-=2H2O+AlO2-。
b.酸性高锰酸钾溶液能氧化亚铁离子,使得高锰酸钾溶液褪色,故答案为:稀硫酸、KMnO4溶液。
考点:本题考查实验基本仪器和基本操作、探究实验方案的设计与分析、离子方程式的书写。


科目:高中化学 来源:2015届广东省湛江市高一第一学期期中考试化学试卷(解析版) 题型:实验题
(16分)实验室为完成某一实验,需用240mL1.0mol/L的稀盐酸,现用11.8mol/L的浓盐酸配制,填空并请回答下列问题:
(1)配制完成某一实验所需1.0mol/L的盐酸溶液,应量取浓盐酸体积为 mL,所用到的玻璃仪器除量筒、烧杯、玻璃棒外还要用到有 、 等。
(2)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次) →D。
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.继续往容量瓶内小心加水,直到液面接近刻度1—2cm处
F.改用某仪器加水,使溶液凹液面恰好与刻度相切
(3)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响):没有进行A操作 ;C操作时不慎有少量液体溅出容量瓶外 ;定容时俯视_____________。
(4)10.6gNa2CO3与足量所配制的盐酸反应,生成CO2气体在标准状况下的体积是__________升。
查看答案和解析>>
科目:高中化学 来源:2015届江苏省盐城市、建湖二中高一上学期期中联考化学试卷(解析版) 题型:选择题
能用来区别NH4Cl、NaCl、Na2CO3三种物质的试剂(必要时可以加热)是
A、AgNO3溶液 B、稀硫酸 C、稀盐酸 D、Ba(OH)2溶液
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
短周期主族元素A、B、C、D、E的原子序数依次增大,其中只有C是金属元素,B是地壳中含量最多的元素,A元素常见化合价为+1和-1;A与C的最外层电子数相同,C、D两元素原子的电子数之和为A、B两种元素原子的电子数之和的3倍。下列叙述正确的是
A.元素的原子半径:A<B<C<D< E
B.对应氢化物的热稳定性:D > E
C.B与C、B与D形成的化合物中化学键类型相同
D.五种元素中最高价氧化物对应的水化物酸性最强的是E
查看答案和解析>>
科目:高中化学 来源:2015届江苏省淮安市高三上学期第一次阶段性测试化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是
A.与Al反应放出H2的溶液:Mg2+、Ca2+、HCO3-、NO3-
B.10 mol·L-1的浓氨水:Al3+、NH4+、NO3-、I—
C.0.1 mol·L-1KMnO4溶液:Na+、Fe2+、SO42-、Cl—
D.c(H+)/c(OH—)=1×10—12的溶液:K+、Na+、AlO2—、CO32—
查看答案和解析>>
科目:高中化学 来源:2015届江苏省、常州一中、沭阳中学高三联合调研化学试卷(解析版) 题型:选择题
室温下,下列叙述正确的是
A.pH=2的HA酸溶液与pH=12的MOH碱溶液以任意比混合:c(H+) + c(M+)=c(OH-) + c(A-)
B.对于0.1mol/LNa2SO3溶液:c(Na+)=2c(SO32-) + c(HSO3-) + 2c(H2SO3)
C.等浓度、等体枳的Na2CO3和NaHCO3混合: >
>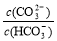
D.将足量AgCl分别放入:①5m水,②10mL0.2mol/LMgC12,③20mL0.3mol/L盐酸中溶解至饱和,c(Ag+):①>②>③
查看答案和解析>>
科目:高中化学 来源:2015届江苏省、常州一中、沭阳中学高三联合调研化学试卷(解析版) 题型:选择题
用下图装置(夹持、加热装置已略)进行试验,有②中现象,不能证实①中反应发生的是

| ①中实验 | ②中现象 |
A | 铁粉与水蒸气加热 | 肥皂水冒泡 |
B | 加热NH4Cl和Ca(OH)2的混合物 | 酚酞溶液变红 |
C | NaHCO3固体受热分解 | 澄清石灰水变浑浊 |
D | 石蜡油在碎瓷片上受热分解 | Br2的CCl4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源:2015届江苏省泰州市姜堰区高二上学期中考试化学试卷(选修)(解析版) 题型:选择题
条件一定时,反应2A(g)+B(g) 2C(g),B的转化率α与温度T变化关系曲线图如下所示,图中4个点中,表示未达到平衡状态,且V正<V逆的点是
2C(g),B的转化率α与温度T变化关系曲线图如下所示,图中4个点中,表示未达到平衡状态,且V正<V逆的点是

A.a B.b C.c D.d
查看答案和解析>>
科目:高中化学 来源:2015届江苏省高三上学期第一次阶段性检测化学试卷(解析版) 题型:选择题
在离子RO42—中,共有x个核外电子,R的质量数为A,则R原子核内含有的中子数目为
A.A-x+48 B.A-x+24 C.A-x+34 D.A-x-24
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com