
分析 (1)Ni的核外电子排布式是1s22s22p63s23p63d 84s2,失去4s能级2个电子形成Ni2+;
(2)CN-与Ni2+之间形成配位键,属于σ键;
解答 解:(1)Ni的核外电子排布式是1s22s22p63s23p63d 84s2,失去4s能级2个电子形成Ni2+,Ni2+的核外电子排布式为:1s22s22p63s23p63d8,
故答案为:1s22s22p63s23p63d8;
(2)CN-与Ni2+之间形成4个配位键,属于σ键,CN-与Ni2+形成1个[Ni(CN)4]2-配离子时新形成 4个σ键,
故答案为:4.
点评 本题考查核外电子排布、配位键,比较基础,根据能量最低原理、洪特规则特例书写核外电子排布式,共价键根据共用电子对偏移分为极性键与非极性、根据电子云重叠分为σ键与π键,根据共用电子对数分为单键、双键与三键.


科目:高中化学 来源: 题型:选择题
| A. | K2CO3 KHCO3 KCl NH4Cl | |
| B. | K2CO3 KHCO3 NH4Cl KCl | |
| C. | (NH4)2SO4 NH4Cl KNO3 K2CO3 | |
| D. | NH4Cl (NH4)2SO4 K2CO3 KNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
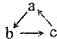 已知abc是中学常见的含有同种元素的三种物质,具有如图的转化关系(“→”表示在一定条件下可一步完成),下列各组物质中,不符合上述转化关系的是( )
已知abc是中学常见的含有同种元素的三种物质,具有如图的转化关系(“→”表示在一定条件下可一步完成),下列各组物质中,不符合上述转化关系的是( )| 选项 对应物质 | A | B | C | D |
| a | Cu(OH)2 | Na2O | Fe | Mg |
| b | CuCl2 | NaCl | FeCl3 | MgO |
| c | Cu | Na | FeCl2 | MgCl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
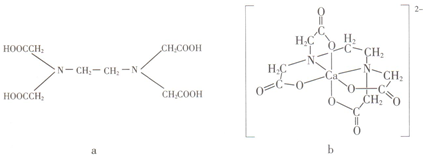
| A. | a和b中的N原子均为sp3杂化 | B. | b中Ca2+的配位数为4 | ||
| C. | b含有分子内氢键 | D. | b含有共价键、离子键和配位键 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铜片消耗完所需时间 | B. | 反应生成的气体体积(标准状况下) | ||
| C. | 反应中氧化剂得到的电子总数 | D. | 反应后溶液中硝酸银离子的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com