
【题目】研究氮的循环和转化对生产、生活有重要价值。
I.氮是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如图所示:

设备1、3中发生反应的化学方程式分别是_________________、_________________;设备2中通入的物质A是__________。
II.氨氮废水的处理是当前科学研究的热点问题之一。氨氮废水中氮元素多以NH4+和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:

(1)过程①的目的是将NH4+转化成NH3,并通过鼓入大量热空气将氨气吹出,写出NH4+转化成NH3的离子方程式:______________________________
(2)过程②中加入NaClO溶液可将氨氮化合物转化为无毒物质,反应后含氮元素、氯元素的物质的化学式分别为__________、__________。
(3)图中含余氯废水中含有NaClO,则X可选用__________(填序号)的溶液达到去除余氯的目的。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
写出该反应的离子方程式:___________________________。
【答案】4NH3+5 O2![]() 4NO+6H2O HNO3+NH3=NH4NO3 O2(或空气) NH4++OH-
4NO+6H2O HNO3+NH3=NH4NO3 O2(或空气) NH4++OH-![]() NH3+H2O N2 NaCl b SO32-+ClO-=SO42-+Cl-
NH3+H2O N2 NaCl b SO32-+ClO-=SO42-+Cl-
【解析】
I.氨气和氧气通入设备1中,在该设备中氨气被催化氧化生成NO和水;之后进入设备2,得到硝酸,NO被氧化,则A为应为氧气;硝酸进入设备3和氨气反应生成硝酸铵。
II.含铵根的废水和NaOH溶液反应生成NH3,之后将铵根浓度较低的废水与NaClO溶液混合,NaClO具有强氧化性,将-3价的N元素氧化无毒的N2,自身被还原成Cl-;再添加适量的还原剂将过量的次氯酸钠除去,得到达标废水。
I.根据分析可知设备1中方程式为4NH3+5 O2![]() 4NO+6H2O;设备3中方程式为HNO3+NH3=NH4NO3;物质A为O2(或空气);
4NO+6H2O;设备3中方程式为HNO3+NH3=NH4NO3;物质A为O2(或空气);
II.(1)NH4+转化成NH3的离子方程式为NH4++OH-![]() NH3+H2O;
NH3+H2O;
(2)根据分析可知含氮元素、氯元素的物质的化学式分别为N2、NaCl;
(3)根据分析可知X应为还原剂,KOH还原性弱,NaCl和次氯酸反应生成有毒的氯气;高锰酸钾为强氧化剂,Na2SO3有较强还原性,且产物无污染,所以选b;离子方程式为SO32-+ClO-=SO42-+Cl-。


科目:高中化学 来源: 题型:
【题目】实验室需要配制0.1molL-1NaOH溶液500mL,回答下列问题:

(1)如图所示的仪器中配制溶液肯定不需要的是___(填字母),配制上述溶液还需要用到的玻璃仪器是___(填仪器名称)。
(2)配制该NaOH溶液,需要用托盘天平称取NaOH固体___克。
(3)将NaOH固体溶解时用到玻璃棒,其作用是___。
(4)在配制过程中,下列实验操作会引起所配的NaOH溶液的浓度偏大的是___。
A.烧杯未进行洗涤
B.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中,并进行定容
C.往容量瓶转移时,有少量液体溅出
D.在容量瓶中定容时俯视容量瓶刻度线
E.摇匀后静置,发现液面不到刻度线,再加水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验过程或事实的反应方程式不正确的是
A. 熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOH![]() Na2SiO3+H2O
Na2SiO3+H2O
B. 在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+ H2O2+2H+= I2+O2↑+2H2O
C. 红热的铁丝与水接触,表面形成蓝黑色(或黑色)保护层:3Fe+ 4H2O(g)![]() Fe3O4+4H2
Fe3O4+4H2
D. “84消毒液”(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气:ClO-+ Cl-+ 2H+= Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某有机化合物A的结构,进行如下实验:
Ⅰ.分子式的确定:
(1)将有机物A置于氧气流中充分燃烧,实验测得生成7.2gH2O和13.2gCO2,消耗氧气10.08L(标准状况),则该物质中各元素的原子个数之比是____________________。
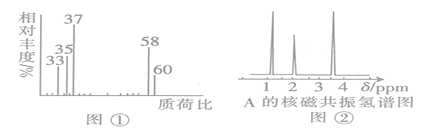
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为________,该物质的分子式是_______________。
(3)根据价键理论,预测A可能的结构简式: _________________________。
Ⅱ.结构式的确定:
(4)核磁共振氢谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值可以确定分子中氢原子的种类和数目。经测定,有机物A的核磁共振氢谱如图②,则A的结构简式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO2是一种重要的化工原料,依据题给信息,回答下列问题:
Ⅰ.碳酸钠可利用CO2采用氨碱法生产
(1)碳酸钠可作为碱使用的原因是_____________(用离子方程式表示)。
(2)已知:①2NaOH(s)+CO2(g)=Na2CO3(s)+H2O(g) ΔH1=127.4 kJ/mol
②NaOH(s)+CO2(g)=NaHCO3(s) ΔH2=131.5kJ/mol
反应2NaHCO3(s)=Na2CO3(s)+ H2O(g) +CO2(g)的ΔH=___________ kJ/mol。
Ⅱ.在体积为2 L的密闭容器中,充入1mol/LCO2 和1mol/L H2,进行如下化学反应:
CO2(g)+H2(g)![]() CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 | |||
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应为____________反应(选填吸热、放热)。
(2)能判断该反应是否达到化学平衡状态的依据是_______________。
a.容器中压强不变 b.混合气体中 c(CO)不变
c. υ正(H2)=υ逆(H2O) d. c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____________℃。
(4)某温度下经2min反应达到平衡后c(CO)=0.8mol/L,此温度下的平衡常数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲胺(CH3NH2)是一种一元弱碱,其电离方程式为:CH3NH2 + H2O ![]() CH3NH3+ + OH-。常温下,向20.0 mL 0.10 mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是
CH3NH3+ + OH-。常温下,向20.0 mL 0.10 mol/L的甲胺溶液中滴加VmL0.10mol/L的稀盐酸,混合溶液的pH与相关微粒浓度的关系如图所示。下列说法中错误的是
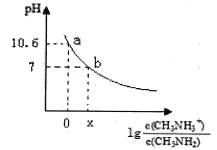
A. b点对应加入盐酸的体积V<20.00mL
B. 常温下,根据a点可知甲胺的电离平衡常数Kb=10 -3.4
C. b点可能存在关系:c(Cl-) > c(CH3NH3+) > c(H+) = c(OH-)
D. V=20.00mL时,溶液呈弱酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在T ℃时,铬酸银(Ag2CrO4)在水溶液中的沉淀溶解平衡曲线如图所示。下列说法中不正确的是
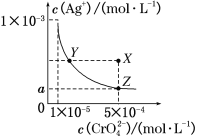
A. T ℃时,在Y点和Z点,Ag2CrO4的Ksp相等
B. 向饱和Ag2CrO4溶液中加入固体K2CrO4不能使溶液由Y点变为X点
C. 图中a=![]() ×10-4
×10-4
D. T ℃时,Ag2CrO4的Ksp为1×10-8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z、Q是原子序数依次增大的前四周期元素,W是宇宙中最丰富的元素;X、Z元素原子基态时,核外电子均排布在3个能级上,且它们的价电子层上均有2个未成对电子;向含有 QSO4的溶液中滴加氨水,生成蓝色沉淀,继续滴加氨水,沉淀溶解,得深蓝色溶液。请回答下列问题:
(1)Y元素在周期表中的位置为___________, Z原子的价电子排布图为___________________
(2)W可分别与X、Y形成多种化合物,其中,最简单化合物的稳定性由强到弱的顺序为_____(用分子式表示);Y的一种氢化物能在卫星发射时作燃料,写出该氢化物的结构式_______________。
(3)继续滴加氨水,沉淀溶解时反应:____________________________(用离子方程式表示),向深蓝色溶液中再加乙醇,会析出深蓝色的[Q(NH3)4]SO4·H2O晶体,该晶体中含有的化学键____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组同学为了探究铜与浓硫酸的反应,进行了一系列实验。在反应过程中会发生一些副反应,生成不溶于水和酸的CuS、Cu2S。
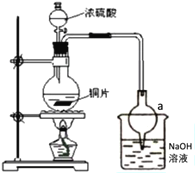
(1)处于安全和绿色化学考虑,在制取硫酸铜时,可选用下列的物质是____。
a.Cu b.CuO c.CuS d.CuSO4·Cu(OH)2H2O
(2)装置a的作用是___。反应过程中,因为浓硫酸的吸水作用,烧瓶中出现白色固体物质,如何简便检验反应后圆底烧瓶里有Cu2+存在?___。在实际反应中,由于条件控制不好,容易产生CuS和Cu2S固体:2CuS![]() Cu2S+S。
Cu2S+S。
(3)已知样品质量为ag,得到Cu2S是bg,则样品中CuS质量分数是___。如果Cu2S高温下转化为Cu,则实验测得的值会___(填“偏大”、“偏小”或“不变”)
(4)根据以上信息,说明铜与浓硫酸反应需要控制哪些条件?___
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com