
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如右图所示)。
 (1)制备实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)。
(1)制备实验开始时,先检查装置气密性,接下来的操作依次是 (填序号)。
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸
(2)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出的下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
丁方案:与足量Zn反应,测量生成的H2体积。
继而进行下列判断和实验:
①判定甲方案不可行,理由是 。
②进行乙方案实验:准确量取残余清液稀释一定的倍数后作为试样。
a.量取试样20.00mL,用0.1000 mol·L—1NaOH标准溶液滴定,消耗22.00mL,该次滴定测的试样中盐酸浓度为 mol·L—1;
b.平行滴定后获得实验结果。
 ③判断丙方案的实验结果 (填“偏大”、“偏小”或“准确”)。
③判断丙方案的实验结果 (填“偏大”、“偏小”或“准确”)。
[已知:Ksp(CaCO3)=2.8×![]() 、Ksp(MnCO3)=2.3×
、Ksp(MnCO3)=2.3×![]() ]
]
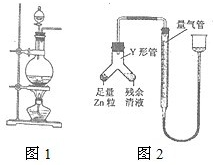
④进行丁方案实验:装置如右图所示(夹持器具已略去)。
(i)使Y形管中的残余清液与锌粒反应的正确操作是将 转移到 中。
(ii)反应完毕,每间隔1分钟读取气体体积、气体体积逐渐减小,直至不变。气体体积逐次减小的原因
是 (排除仪器和实验操作的影响因素)。
解析:(1)加药顺序一般是先加入固体药品,再加入液药品,最后再加热。则依次顺序是ACB。考查实验的细节,看学生是否真的做过实验,引导实验课要真正地上,而不是在黑板上画。
(2)①加入足量的硝酸银溶液只能求出氯离子的量,而不能求出剩余盐酸的浓度。
②由CHClVHCl=CNaOHVNaOH可得出盐酸的浓度为0.1100mol/L,这是简单的中和滴定计算。
③根据题意碳酸锰的Ksp比碳酸钙小,其中有部分碳酸钙与锰离子反应转化成碳酸锰沉淀,剩余的碳酸钙质量变小,多消耗了碳酸钙,但是由此计算得出盐酸的浓度就偏大了(疑问)。如果将题目改成“称量剩余的固体质量”,由于部分碳酸钙与转化成碳酸锰沉淀,称量剩余的固体质量会偏大,这样一来反应的固体减少,实验结果偏小!
④使Zn粒进入残余清液中让其发生反应。这样残余清液就可以充分反应,如果反过来,残余清液不可能全部转移到左边。反应完毕时,相同时间内则气体体积减少,又排除了其它影响因素,只能从气体本身角度思考,联想到该反应是放热的,就可能想到气体未冷却了。
实验题总体比较基础简单,可能最后一问比较出人意料,难以想到。


科目:高中化学 来源: 题型:阅读理解
 (2012?福建)实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图1所示).
(2012?福建)实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图1所示).查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1所示).
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如图1所示).查看答案和解析>>
科目:高中化学 来源:上海市长宁区2013年高考一模化学试题 题型:058
实验室常用MnO2与浓盐酸反应制备Cl2(反应装置如下图所示).

1.制备实验开始时,先检查装置气密性,接下来的操作依次是(填序号).
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸
制备反应会因盐酸浓度下降而停止.为测定已分离出过量MnO2后的反应残余液中盐酸的浓度,探究小组同学提出的下列实验方案∶
甲方案∶与足量AgNO3溶液反应,称量生成的AgCl质量.
乙方案∶与已知量CaCO3(过量)反应,称量剩余固体的质量.
丙方案∶与足量Zn反应,测量生成的H2体积.
继而进行下列判断和实验∶
2.判定甲方案不可行,理由是________.
3.乙方案的实验发现,固体中含有MnCO3,说明碳酸钙在水中存在________,测定的结果会∶(填“偏大”、“偏小”或“准确”).
进行丙方案实验∶装置如下图所示(夹持器具已略去).

4.使Y形管中的残余清液与锌粒反应的正确操作是将转移到________中.
5.反应完毕,每间隔1分钟读取气体体积,发现气体体积逐渐减小,直至不变.气体体积逐次减小的原因是________(排除装置和实验操作的影响因素).
6.小组内又有同学提出还可采用酸碱中和滴定法测定残余液中盐酸的浓度,但还需经查阅资料知道∶________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com