
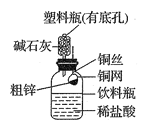
【题目】某化学兴趣小组拟用下图装置测定某粗锌样品中锌的质量分数。他们查阅资料后获知该粗锌样品中的其他成分不能与稀盐酸反应。请填写以下实验报告。
(1)实验目的: 。
(2)实验步骤:
①称取10.0g粗锌置于铜网中,按图示装置组装后,称得仪器和药品总质量为120.0g。
②将铜网插入足量的稀盐酸中,有关反应的化学方程式为 。
③反应完全后,称得装置总质量为119.8g,则粗锌中锌的质量分数为 。
(3)问题探究:(已知碱石灰是NaOH和CaO的混合物,常用于干燥、吸收气体)
①该实验若不用碱石灰,则所测得的粗锌中锌的质量分数将 (填“偏大”、“偏小”或“无影响”);
②若将粗锌换成某含有杂质的石灰石样品(杂质也不与稀盐酸反应),判断该实验方案能不能用于石灰石样品中CaCO3质量分数的测定,并说明理由____________________。
【答案】(1)测定粗锌样品中锌的质量分数(或纯度)
(2)②Zn+2HCl=ZnCl2+H2↑③65%
(3)①偏大②不能,碱石灰能吸收反应生成的CO2
【解析】
试题分析:(1)根据题意可知该实验的所以目的是测定粗锌样品中锌的质量分数;
(2)由于粗锌中的杂质不与稀盐酸反应,Cu也不与稀盐酸反应,所以发生的反应只有Zn与稀盐酸的反应,化学方程式为Zn+2HCl=ZnCl2+H2↑;原装置的总质量是120.0g,反应完全后变为119.8g,说明产生的氢气的质量是120.0-119.8=0.2g,其物质的量是0.1mol,则参加反应的Zn的物质的量是0.1mol,质量是0.1mol×65g/mol=6.5g,所以粗锌中锌的质量分数是![]() ×100%=65%;
×100%=65%;
(3)①若该实验中不用碱石灰,则放出的氢气会带走部分的水蒸气,造成反应完全后整个装置的质量减少,即反应前后装置的质量差偏大,产生的氢气偏多,所以所测得的粗锌中锌的质量分数将偏大;②若将粗锌换成某含有杂质的石灰石样品,由于石灰石与盐酸反应产生二氧化碳气体,碱石灰也能吸收二氧化碳,不能确定氢气的质量,所以不能测定粗锌中锌的质量分数,因此不能将粗锌换成某含有杂质的石灰石样品。


科目:高中化学 来源: 题型:
【题目】铈、铬、钛、镍虽不是中学阶段常见的金属元素,但在工业生产中有着重要作用。
(1)二氧化铈 (CeO2)在平板电视显示屏中有着重要应用。CeO2在稀硫酸和H2O2的作用下可生成Ce3+,CeO2在该反应中作__________剂。
(2)自然界Cr主要以+3价和+6价存在。+6价的Cr能引起细胞的突变,可以用亚硫酸钠将其还原为+3价的铬。完成并配平下列离子方程式:
_____Cr2O72-+_____SO32-+_____ =_____Cr3++_____SO42-+ _____H2O
(3)钛(Ti)被誉为“二十一世纪的金属”,工业上在550℃时用钠与四氯化钛反应可制得钛,该反应的化学方程式是 。
(4)NiSO4·xH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如下:
①向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质,除去Cu2+的离子方程式为_____________________。
②对滤液Ⅱ先加H2O2再调pH,调pH的目的是 _。
③滤液Ⅲ溶质的主要成分是NiSO4,加Na2CO3过滤后,再加适量稀硫酸溶解又生成NiSO4,这两步操作的目的是_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法中,不正确的是( )
A.液化石油气和天然气的主要成分都是甲院
B.苯、乙醇和乙酸都能发生取代反应
C.油脂在碱的催化作用下可发生水解,工业上利用该反应生产肥皂
D.煤的气化是化学变化,石油分馏是物理变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)3 mol二氧化碳气体中,约含有 个二氧化碳分子;2molNH4+中共有 mol电子,与之电子数相等的H2O的质量是 ,这些水若完全电解,产生的氢气在标准状况下的体积为 L。
(2)相同质量的氧气、氢气、二氧化碳中,含有分子数目最少的是 (填化学式,下同),标准状况下体积最大的是 ,原子数最少的是 。
(3)在NaCl与MgCl2的混合液中,Na+与Mg2+的物质的量之比为1:2。如果混合液中共有0.5 mol Cl-,溶液的体积为0.5 L,则混合液中氯化钠的质量为 ;MgCl2的物质的量浓度为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如右图所示,对该反应的推断合理的是( )
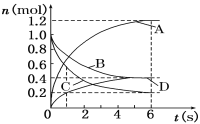
A.该反应的化学方程式为3B+4D ![]() 6A+2C
6A+2C
B.反应进行到1 s时,v(A)=v(D)
C.反应进行到6 s时,B的平均反应速率为0.05 mol/(L·s)
D.反应进行到6 s时,各物质的反应速率相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】己知:
(1)Al(OH)3的电离方程式:AlO2-+H++H2O![]() Al(OH)3
Al(OH)3![]() A13++3OH-
A13++3OH-
(2)无水AlCl3晶体的沸点:182.9℃,溶于水的电离方程式为:AlCl3=Al3++3Cl-
(3)PbSO4难溶于水,易溶于醋酸钠溶液,反应的化学方程式为:PbSO4+2CH3COONa=Na2SO4+(CH3COO)2Pb
则下列关于A1(OH)3、AlCl3和(CH3COO)2Pb的说法中正确的是( )
A.均为强电解质 B.均为弱电解质
C.均为离子化合物 D.均为共价化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 向某钠盐溶液中滴加稀硫酸 | 产生能使石灰水变浑浊的气体 | 该溶液一定含有CO或HCO |
B | KIO3溶液中加入HI溶液,并加入淀粉 | 溶液变蓝色 | KIO3的氧化性比I2强 |
C | 向Na2S溶液中滴加盐酸 | 产生臭鸡蛋气味的气体 | 氯的非金属性比硫的强 |
D | CO还原Fe2O3得到的黑色固体加入盐酸溶解后,再加入KSCN溶液 | 溶液不显红色 | 黑色固体中无Fe3O4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com