
| A. | 28gCO和N2混合气体中含有原子总数为2NA | |
| B. | 在1L1mol•L-1的氨水中含有NA个NH3分子 | |
| C. | 标准状况下,11.2LNO和11.2LO2混合后气体分子数为NA | |
| D. | 1mol Fe分别与足量Cl2、S反应,Fe失去电子数都为2NA |
分析 A.CO和N2摩尔质量都是28g/mol,都双原子分子;
B.氨气与水反应生成一水合氨,部分一水合氨电离生成氨根离子和氢氧根离子;
C.一氧化氮和氧气发生反应生成二氧化氮,二氧化氮聚合为四氧化二氮;
D.铁与氯气反应生成氯化铁,与硫反应生成硫化亚铁.
解答 解:A.28gCO和N2混合气体的物质的量为1mol,含有原子总数为2NA,故A正确;
B.氨气与水反应生成一水合氨,部分一水合氨电离生成氨根离子和氢氧根离子,所以在1L1mol•L-1的氨水中含有小于NA个NH3分子,故B错误;
C.一氧化氮和氧气发生反应生成二氧化氮,标况下11.2LNO物质的量=$\frac{11.2L}{22.4L/mol}$=0.5mol,11.2LO2物质的量为0.5mol,混合后反应2NO+O2=2NO2,得到0.5molNO2,0.25molO2,二氧化氮聚合为四氧化二氮,所得气体分子数小于0.75NA,故C错误;
D.1mol Fe分别与足量Cl2、S反应,Fe失去电子数都分别为3NA、2NA,故D错误;
故选:A.
点评 本题考查了阿伏伽德罗常数的分析应用,熟练掌握公式的使用和物质的结构是解题关键,注意铁与氯气、硫反应得到化合物中铁元素化合价不同,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L NH4HCO3溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3- )>c(OH-) | |
| B. | 20ml 0.1mol/L CH3COONa溶液与10ml 0.1mol/LHCl溶液混合后溶液呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(H+) | |
| C. | 室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)+c(H+)>c(NH4+ )>c(OH-) | |
| D. | 0.1mol/L CH3COOH溶液与0.1mol/L NaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+c(CH3COOH) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ②③④ | C. | ①②③④ | D. | ①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
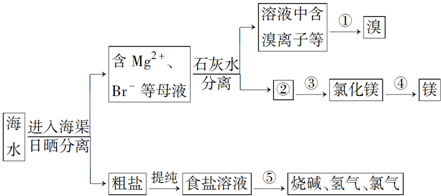
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温时在水中的溶解性:NaHCO3>Na2CO3 | |
| B. | 热稳定性:NaHCO3<Na2CO3 | |
| C. | 与酸反应的快慢:NaHCO3<Na2CO3 | |
| D. | Na2CO3不能转化成NaHCO3,而NaHCO3能转化成Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 | |
| B. | 在0.1mol•L-1 的NaHA溶液pH=4,则H2A为强酸 | |
| C. | 常温下,pH=7的NH4Cl与氨水的混合溶液中:c(Clˉ)>c(NH4+)>c(H+)=c(OHˉ) | |
| D. | 向0.1mol•L-1的氨水中加入少量硫酸铵固体,则溶液中c(OH-)/c(NH3•H2O)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 从海水中富集含微量元素的化合物 | B. | 使含微量元素的离子沉淀 | ||
| C. | 对含微量元素的混合物进行提纯 | D. | 从化合物中冶炼这些单质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com