
| A���ۢܢ� | B���ڢ� | C���٢� | D���٢ۢܢ� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������� | B���������� | C��������� | D��������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��0 |
| B��1 |
| C��2 |
| D��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
A��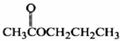 | B��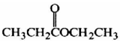 | C��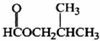 | D��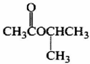 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NO(g) ��H ��0
2NO(g) ��H ��0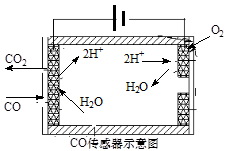
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ࡢ��֬�������ʶ��Ǹ߷��ӻ����� |
| B������ˮ������ղ����������� |
| C����֬��ˮ�ⷴӦ��Ϊ������Ӧ |
| D�����Ȼ�ʹ�����ʱ��ԣ����ʳ�������������Ӫ����ֵ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ֲ���Ͳ��ܷ���ˮ�ⷴӦ | B������ˮ������ղ����������� |
| C���������ܷ���������Ӧ��ˮ�ⷴӦ | D��������ˮ��IJ���Ϊ������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
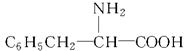 )�ж���ͬ���칹�塣����ͬʱ���������������������д�����ȡ�����ı���������һ������ֱ�������ڱ����ϵ��칹����(����)
)�ж���ͬ���칹�塣����ͬʱ���������������������д�����ȡ�����ı���������һ������ֱ�������ڱ����ϵ��칹����(����)| A��3�� | B��5�� | C��6�� | D��10�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com