
【题目】(题文)阿托酸乙酯可用于辅助胃肠道痉挛及溃疡。阿托酸乙酯的一种合成路线如下图所示: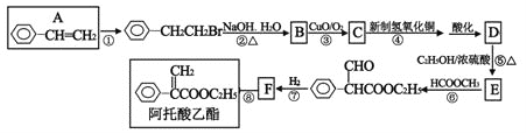
请回答下列问题:
(1)A的命名____________ E的分子式为_________F的结构简式_________ ①的反应类型_______
(2)在反应①②③④⑤⑥⑦⑧中,属于取代反应的有_____________;
(3)反应③的方程式_________________________________________。
(4)有关阿托酸乙酯的说法正确的是 (_______)
A.能使高锰酸钾褪色,不能使溴水褪色
B.1mol阿托酸乙酯最多能与4molH2加成
C.能发生加成、加聚、氧化、水解等反应
D.分子式为C11H13O2
(5)D的同分异构体有多种,符合含有苯环且能与碳酸氢钠反应放出气体的同分异构体有_________种(不包含D)。
【答案】 苯乙烯 C10H12O2 ![]() 加成反应 ②⑤⑥
加成反应 ②⑤⑥ ![]() BC 3
BC 3
【解析】由题中各物质的转化关系可知,A与溴化氢发生加成反应生成![]() ,
,![]() 在碱性条件下水解,发生取代反应生成B为
在碱性条件下水解,发生取代反应生成B为![]() ,B发生氧化反应生成C为
,B发生氧化反应生成C为![]() ,C再被氧化、酸化后得D为
,C再被氧化、酸化后得D为![]() ,D与乙醇发生取代反应生成E为
,D与乙醇发生取代反应生成E为![]() ,E与甲酸甲酯发生取代反应生成
,E与甲酸甲酯发生取代反应生成![]() ,
,![]() 与氢气发生加成反应生成F为
与氢气发生加成反应生成F为![]() ,F再发生消去反应得阿托酸乙酯,据此答题。
,F再发生消去反应得阿托酸乙酯,据此答题。
由题中各物质的转化关系可知,A与溴化氢发生加成反应生成![]() ,
,![]() 在碱性条件下水解,发生取代反应生成B为
在碱性条件下水解,发生取代反应生成B为![]() ,B发生氧化反应生成C为
,B发生氧化反应生成C为![]() ,C再被氧化、酸化后得D为
,C再被氧化、酸化后得D为![]() ,D与乙醇发生取代反应生成E为
,D与乙醇发生取代反应生成E为![]() ,E与甲酸甲酯发生取代反应生成
,E与甲酸甲酯发生取代反应生成![]() ,
,![]() 与氢气发生加成反应生成F为
与氢气发生加成反应生成F为![]() ,F再发生消去反应得阿托酸乙酯,(1)A为
,F再发生消去反应得阿托酸乙酯,(1)A为![]() ,命名为苯乙烯;E为
,命名为苯乙烯;E为![]() ,E的分子式为C10H12O2,F的结构简式为
,E的分子式为C10H12O2,F的结构简式为![]() ,反应①是
,反应①是![]() 与溴化氢发生加成反应生成
与溴化氢发生加成反应生成![]() ,反应类型为加成反应;(2)在反应①②③④⑤⑥⑦⑧中,属于取代反应的有②⑤⑥;(3)反应③的方程式为2
,反应类型为加成反应;(2)在反应①②③④⑤⑥⑦⑧中,属于取代反应的有②⑤⑥;(3)反应③的方程式为2![]() +O2
+O2![]() 2
2![]() +2H2O;(4)阿托酸乙酯中有酯基、碳碳双键、苯环等结构,所以有关阿托酸乙酯的说法中,A.能使高锰酸钾褪色,不能使溴水褪色,因为能与溴加成,选项A错误;B.1mol阿托酸乙酯最多能与4molH2加成,选项B正确;C.能发生加成、加聚、氧化、水解等反应,选项C正确;D.分子式为C11H13O2,因为氢原子数不可能为奇数,选项D错误;答案选BC;(5)D的同分异构体有多种,符合含有苯环且能与碳酸氢钠反应放出气体,即有羧基的同分异构体为苯环上连有-CH3和-COOH,它们互为邻间对的关系,所以共有3种(不包含D)。
+2H2O;(4)阿托酸乙酯中有酯基、碳碳双键、苯环等结构,所以有关阿托酸乙酯的说法中,A.能使高锰酸钾褪色,不能使溴水褪色,因为能与溴加成,选项A错误;B.1mol阿托酸乙酯最多能与4molH2加成,选项B正确;C.能发生加成、加聚、氧化、水解等反应,选项C正确;D.分子式为C11H13O2,因为氢原子数不可能为奇数,选项D错误;答案选BC;(5)D的同分异构体有多种,符合含有苯环且能与碳酸氢钠反应放出气体,即有羧基的同分异构体为苯环上连有-CH3和-COOH,它们互为邻间对的关系,所以共有3种(不包含D)。


科目:高中化学 来源: 题型:
【题目】我国古代中药学著作《新修本草》中关于“青矾”的描述为:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色。”明末学者方以智所著《物理小识》中说:“青矾厂气熏人,衣服当之易烂,栽术不茂。”下列有关叙述正确的是
A. 赤色固体可能是Fe2O3 B. “青矾厂气“可能是CO和CO2
C. 青矾可能是NH4Al(SO4)2·12 H2O D. 青矾宜密闭贮藏,防止还原变质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计了一组实验验证元素周期律。
Ⅰ.为了用实验的方法验证镁和铝的金属性强弱,学生甲和学生乙分别设计了两种不同的方法:
方案一:学生甲用水作试剂,比较镁和铝与水反应的情况
方案二:学生乙用稀盐酸作试剂,比较镁和铝与稀盐酸反应的情况
(1)以上两实验方案实验现象较为明显的是方案___________________________。
(2)学生乙在实验中取了一段黑色的镁带,投入稀盐酸中,现象不十分明显,请分析原因____。
(3)学生内另辟蹊径,不用镁、铝的单质,而用镁、铝的可溶盐及一些其它化学试剂,进行实验也得出正确的结论,简述学生丙用的是什么方法?_____________________________。
Ⅱ.学生丁设计了下图装置以验证硫、碳、硅元素的非金属性强弱。已知B是一种正盐,是工业生成玻璃的主要原料之一。

(1)写出所选用物质的化学式:A:__________________,B:____________________。
(2)写出烧杯中发生反应的离子方程式:_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质,不能按![]() (“→”表示反应一步完成)关系转化的是( )
(“→”表示反应一步完成)关系转化的是( )
选项 | a | b | c |
A | Al2O3 | Na[Al(OH)4] | Al(OH)3 |
B | AlCl3 | Al(OH)3 | Na[Al(OH)4] |
C | Al | Al(OH)3 | Al2O3 |
D | MgCl2 | Mg(OH)2 | MgO |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某含氧有机化合物可以作为无铅汽油的抗爆震剂,其相对分子质量为88.0,含C的质量分数为0.682,含H的质量分数为0.136,其余为O。
(1)试确定该化合物的分子式______。(写出计算过程)
(2)经红外光谱和核磁共振氢谱显示该分子中有4个甲基。请写出其结构简式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肼是一种强还原剂,用NaClO与NH3反应可用于生产肼(N2H4),其反应的化学方程式为:NaClO+2NH3= N2H4+NaCl+H2O。
⑴生产1000 g质量分数为25.6%的肼溶液最少需要___________L(标准状况)NH3。
⑵工业次氯酸钠溶液中含有氯酸钠会影响所得肼的产品质量。测定次氯酸钠样品中的氯酸钠含量的方法如下:取10.00 mL 碱性NaClO溶液试样,加入过量H2O2,将次氯酸钠完全还原(ClO3-在酸性条件下具有强氧化性,但碱性条件下几乎无氧化性),加热煮沸,冷却至室温,加入硫酸至酸性,再加入0.1000 mol·L-1 硫酸亚铁标准溶液30.00 mL,充分反应后,用0.01000 mol·L-1酸性K2Cr2O7溶液滴定至终点(Cr2O72-被还原为Cr3+),消耗该溶液20.00 mL。
①用H2O2与次氯酸钠反应的离子方程式为___________。
②实验中加热煮沸的目的是___________。
③计算样品中NaClO3的含量(以g·L-1表示),写出计算过程。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子能大量共存的是( )
A.Ca2+、HCO3-、K+、NO3-B.HCO3-、H+、Ba2+、Na+
C.HCO3-、OH-、Al3+、Na+D.Mg2+、Fe3+、OH-、Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com