
| A. | 石墨和金刚石的转化是物理变化 | |
| B. | C(s、石墨)=C(s、金刚石)△H=+1.9 kJ•mol-1 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | 1 mol石墨的总键能比1 mol金刚石的总键能小 |
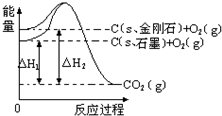
分析 先根据图写出对应的热化学方程式,然后根据盖斯定律写出石墨转变成金刚石的热化学方程式,根据物质的能量越低越稳定,拆化学键吸收能量,形成化学键放出热量来分析.
解答 解:由图得:①C(S,石墨)+O2(g)=CO2(g)△H=-393.5kJ•mol-1,
②C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJ•mol-1,
利用盖斯定律将①-②可得:C(S,石墨)=C(S,金刚石)△H=+1.9kJ•mol-1,则:
A、金刚石和石墨是两种不同的物质,故石墨和金刚石的转化为化学变化,故A错误;
B、根据图示写出热化学方程式后,利用盖斯定律可得:C(S,石墨)=C(S,金刚石)△H=+1.9kJ•mol-1,故B正确;
C、由于石墨转化为金刚石吸热,故石墨的能量更低,而物质的能量越低物质越稳定,故石墨比金刚石更稳定,故C错误;
D、由于)△H=+1.9kJ•mol-1=1mol石墨的总键能-1mol金刚石的总键能,故1mol石墨的总键能比1mol金刚石的总键能大,故D错误.
故选B.
点评 本题考查热利用盖斯定律书写热化学方程式、物质的能量越低越稳定,题目难度不大,注意物质的稳定性与能量的关系.


科目:高中化学 来源: 题型:选择题
| A. | 丙烷分子的球棍模型: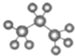 | B. | S的结构示意图为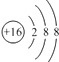 | ||
| C. | HClO的结构式为H-Cl-O | D. | 碳-14核素:814C |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在常温常压下,11.2LO2含有的分子数为0.5NA | |
| B. | 71gCl2所含原子数为2NA | |
| C. | 标准状况下,22.4LH2O含有的分子数为1NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不能发生丁达尔效应的分散系有氯化钠溶液、水等 | |
| B. | 将1L 2mol•L-1的FeCl3溶液制成胶体后,其中含有氢氧化铁胶粒数为2NA | |
| C. | 黄河入海口处三角洲的形成与胶体性质有关 | |
| D. | 将饱和FeCl3溶液加热至沸腾,制得Fe(OH)3胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
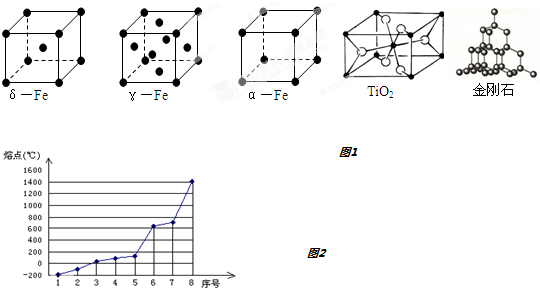
| 共价键 | C-C | O=O | C=O |
| 键能/kJ•mol-1 | a | b | c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com