
| A. |  氢氧化钠溶液 | B. | 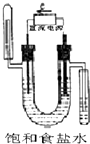 淀粉碘化钾溶液 | C. |  氢氧化钠溶液 | D. |  淀粉碘化钾溶液 |
分析 惰性电极电解食盐水的生成物是氢气、氢氧化钠和氯气.其中氢气在阴极产生,且氢气的密度小于空气的用向下排空气法收集.而氯气在阳极产生,且具有强氧化性,能把碘化钾氧化生成单质碘,碘于淀粉显蓝色,以此解答该题.
解答 解:电解饱和食盐水时,阳极的电极反应式为2Cl--2e-=Cl2↑,用KI淀粉溶液检验产生的Cl2;阴极的电极反应式为2H++2e-=H2↑,阴极有H2生成.结合图中电子从直流电源负极流向电解池阴极,B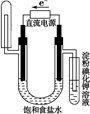 中左侧为阴极,左端用向下排空气法收集H2,为阴极.A、C项中NaOH溶液不能检验是否生成Cl2.
中左侧为阴极,左端用向下排空气法收集H2,为阴极.A、C项中NaOH溶液不能检验是否生成Cl2.
故选B.
点评 本题考查电解原理及物质检验,为高频考点,把握发生的电极反应、物质的检验方法为解答的关键,侧重分析与应用能力的考查,注意氯气的检验方法,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Mg3N2晶体中的化学键是共价键 | |
| B. | 某物质含有离子键,则该物质在任何条件下均能导电 | |
| C. | 干冰是分子晶体,其气化过程中只需克服分子间作用力 | |
| D. | 常温常压下,气态单质分子中,每个原子的最外层都具有8电子稳定结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②④⑤⑦ | B. | ⑥ | C. | ⑥⑦ | D. | ⑤⑥⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应进行60s时,X、Y、Z的浓度相等 | |
| B. | 反应进行80s时,逆反应速率大于正反应速率 | |
| C. | 以X浓度变化表示的反应速率为0.06mol/(L•min) | |
| D. | 反应进行80s时,Y物质的量浓度为0.03mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
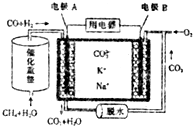
| A. | 电流方向:由B极经用电器流向A极 | |
| B. | 电极B上发生的电极反应为2CO2+O2+4e-═CO22- | |
| C. | 电池工作时,K+、Na+向电极B移动 | |
| D. | 若消耗电极B上的O233.6L(标准状况),则至少需要1moL CH4参加反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O2只作氧化剂 | |
| B. | 2 mol FeSO4发生反应时,反应中共有8 mol电子转移 | |
| C. | 每生成16g氧气就有1mol Fe2+ 被还原 | |
| D. | Na2FeO4既是还原产物又是氧化产物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 9.0g草酸中共用电子对数目为0.9NA | |
| B. | 9.0 g草酸被NaClO氧化生成CO2,转移的电子数为0.2 NA | |
| C. | 9.0 g草酸溶于水,其中C2O42-和HC2O4-的微粒数之和为0.1NA | |
| D. | 9.0g草酸受热完全分解为CO2、CO、H2O,标况下测得生成的气体体积为4.48 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为防止水解,FeCl3溶液中加入少量稀硫酸 | |
| B. | 少量的钠保存在煤油中 | |
| C. | 氢氧化钠溶液保存在具有橡皮塞的玻璃试剂瓶中 | |
| D. | 新制的氯水通常保存在棕色玻璃试剂瓶中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(NH4+)相等的(NH4)2SO4溶液,(NH4)2CO3溶液和NH4Cl溶液:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl) | |
| B. | 0.1 mol/L的HCOOH溶液中:c(HCOO-)+c(OH-)=c(H+) | |
| C. | 0.1mol/L某二元弱酸强碱盐NaHA溶液中:c(Na+)=c(A2-)+c(HA-)+c(H2A) | |
| D. | 10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com