
【题目】现有M、N两种气态化合物,其摩尔质量之比为2:1,试回答下列问题:
(1)同温同压下,M、N气体的密度之比为____________。
(2)相同温度下,在两个相同体积的密闭容器中分别充入M、N,若两个容器中气体的密度相等,则两个容器中的压强之比为____________。
(3)将M、N两种气体分别溶于水(M、N与水均不反应)配成溶液,当两种溶液的质量分数相同时,其密度分别为d1和d2,则两种溶液的物质的量浓度之比为___________。
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案科目:高中化学 来源: 题型:
【题目】对H2在O2中燃烧的反应,下列说法不正确的是 ( )
A.该反应为吸热反应
B.该反应为放热反应
C.断裂H—H键吸收能量
D.生成H—O键放出能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工农业生产和生活中常常进行分离或提纯,请选择相应的方法代号填入空白处:
a.过滤 B.蒸馏 C..萃取 d分液
①分离水和菜籽油的混合物 。②海水淡化 。
(2)如图,两瓶体积相等的气体,在同温、同压下,原子总数 (填“相等”、“不相等”),当两瓶气体质量相等时,N2和O2的体积比为 。
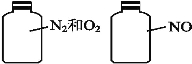
(3)下列物质所含分子数由多到少的顺序是 。(用A、B、C、D排序)
A.标准状况下33.6 L CO
B.所含电子为4 mol的H2
C.20 ℃时45 g H2O
D.常温下,0.5NA个CO2与0.5NA个CO的混合气体
(4)与50 mL 1mol·L-1 MgCl2溶液中的Cl-物质的量浓度相等的是
A.50 mL 1 mol·L-1 FeCl3溶液
B.25 mL 2 mol·L-1 CaCl2溶液
C.50 mL 2 mol·L-1 KCl溶液
(5)某状况下气体摩尔体积为Vm L/mol, 将a L NH3溶解于水中形成b mL氨水溶液,所得溶液的密度为ρ g/cm3,则氨水的溶质质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一恒容密闭容器中充入2mol SO2和1mol O2,在一定条件下发生反应:2SO2+O2![]() 2SO3下列有关说法正确的是( )
2SO3下列有关说法正确的是( )
A.达到化学平衡时,正反应和逆反应的速率都为零
B.当O2的浓度不变时,反应达到平衡状态
C.当单位时间消耗a mol O2,同时消耗2a mol SO2时,反应达到平衡状态
D.当SO2、O2、SO3的分子数比为2:1:2,反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用光洁的铂丝蘸取无色溶液在无色灯焰上灼烧时观察到黄色火焰,下列叙述正确的是( )
A. 只含有Na+ B. 一定含Na+,也可含K+
C. 既含Na+又含有K+ D. 可能含Na+或K+中一种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源环保领域有广泛用途。用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的装置如图所示。下列推断合理的是( )

A. 铁是阳极,电极反应为Fe-6e-+4H2O=FeO42-+ 8H+
B. 电解时电子的流动方向为:负极→Ni电极→溶液→Fe电极→正极
C. 若隔膜为阴离子交换膜,则OH-自右向左移动
D. 电解时阳极区pH降低、阴极区pH升高,撤去隔膜混合后,与原溶液比较pH降低(假设电解前后体积变化忽略不计)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)═CO2(g)+3H2(g)△H=+49.0kJmol﹣1
②CH3OH(g)+O2(g)═CO2(g)+2H2(g)△H=﹣192.9kJmol﹣1
下列说法正确的是( )

A.CH3OH的燃烧热(△H)为﹣192.9kJmol﹣1
B.反应①中的能量变化如图所示
C.CH3OH转变成H2的过程一定要吸收能量
D.根据②推知反应:CH3OH(l)+O2(g)
=CO2(g)+2H2(g)的△H>﹣192.9kJmol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用石墨电极电解CuSO4和KNO3的混合溶液500mL,经一段时间电解后,两极都得到11.2L气体(标准状况下体积),则此混合液中硫酸铜的物质的量浓度为 ( )
A.0.5 mol / L B.0.8 mol / L C.1 mol / L D.1.5 mol / L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关混合物分离与提纯的方法广泛用于实验研究和生产。
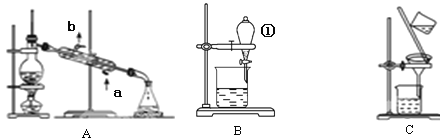
根据上图装置回答下列问题:
(1)若用装置A分离CCl4和溴苯的混合物(已知CCl4和溴苯互溶,沸点分别为76.75℃和156.2℃),在实验时冷却水从冷凝管的 (填“a”或“b”)端通入;温度计读数为80℃时,锥形瓶中收集到的物质是 。
(2)装置B中仪器①的名称是 ,用装置B分离混合物时,为使液体顺利流下,应进行的操作是 。
(3)粗盐中含有少量泥沙、MgCl2、CaCl2及硫酸盐,将粗盐溶解后,先用装置C将泥沙除去,除去泥沙后还需进一步提纯,粗盐提纯步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④调节溶液PH等于7;⑤溶解;⑥过滤;⑦蒸发。正确的操作顺序是 。
A.⑤②③①⑥④⑦ B.⑤①②③⑥④⑦ C.②①③④⑥⑦ D.⑤③②①⑥④⑦
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com