
【题目】下列叙述正确的是
①氧化还原反应的实质是电子的得失。
②若1 mol气体的体积为22.4 L,则它一定处于标准状况下。
③标准状况下,1 L HCl和1 L H2O的物质的量相同。
④溶于水得到的溶液可以导电的物质就是电解质。
⑤利用丁达尔现象区别溶液和胶体。
⑥两种物质的物质的量相同,则它们在标准状况下的体积也相同。
⑦在同温同体积时,气体物质的物质的量越大,则压强越大。
⑧同温同压下,气体的密度与气体的相对分子质量成正比。
A.①②③④B.②③⑥⑦⑧C.⑤⑦⑧D.④⑤⑦⑧
【答案】C
【解析】
①氧化还原反应的实质是电子的得失或电子对的偏移,与题意不符,错误。
②若1 mol气体的体积为22.4 L,根据PV=nRT,则它可能处于标准状况下,与题意不符,错误。
③标准状况下,HCl为气体,H2O为液体, 则1 LH2O的物质的量大于 1 LHCl的物质的量,与题意不符,错误。
④溶于水得到的溶液,可能为溶质与水反应生成的物质导电,也可能该物种电离产生的离子导电,则无法判断该物质就是电解质,与题意不符,错误。
⑤胶体具有丁达尔现象,而溶液无此性质,可利用丁达尔现象区别溶液和胶体,符合题意,正确。
⑥两种物质的物质的量相同,若两物质均为气体,则它们在标准状况下的体积也相同,与题意不符,错误。
⑦在同温同体积时,气体的物质的量之比等于压强之比,则气体物质的物质的量越大,则压强越大,符合题意,正确。
⑧同温同压下,气体的体积之比等于物质的量之比,ρ=![]() 、m=nM,则气体的密度与气体的相对分子质量成正比,符合题意,正确。
、m=nM,则气体的密度与气体的相对分子质量成正比,符合题意,正确。
综上所述,答案为C。


科目:高中化学 来源: 题型:
【题目】下列化学用语正确的是( )
A. (NH4)2 Fe(SO4)2 溶解于水:(NH4)2 Fe(SO4)2 =NH4+ + Fe2 + + 2SO42-
B. Al(OH)3在水中的电离:Al(OH)3 ![]() Al3 ++3OH-
Al3 ++3OH-
C. H3PO4溶解于水:H3PO4 ![]() 3H+ + PO43-
3H+ + PO43-
D. NaHSO4在水中的电离:NaHSO4 = Na+ + NaHSO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有X、Y、Z、W四种短周期主族元素,原子序数依次增大,元素性质与原子(或分子)结构如下表所示:
元素编号 | 元素性质与原子(或分子)结构 |
X | 原子核内没有中子 |
Y | 常温下单质为双原子分子,分子中含有3对共用电子对 |
Z | 最内层电子数是最外层的2倍 |
W | 本周期元素中原子半径最小 |
请回答:
(1)写出元素Z在周期表中的位置______,画出元素W的原子结构示意图______。
(2)Y与W相比,气态氢化物稳定性较弱的是________(填化学式,下同),两元素最高价氧化物对应水化物酸性更强的是__________。
(3)X、Y、Z三种元素可以形成化合物ZYX2,可与化合物XW发生反应,生成两种盐,写出该反应的化学方程式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件的水溶液中不能大量共存的粒子组是( )
A.在碱性溶液中:Na+、K+、![]()
![]()
B.既能溶解Al(OH)3又能溶解H2SiO3的溶液中:Na+、![]() 、ClO-、
、ClO-、![]()
C.含Fe3+的溶液:Na+、Mg2+、![]() 、I-
、I-
D.CH3COOH溶液:![]() 、Cl-、Cu2+、
、Cl-、Cu2+、![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条;F中为红色的铜网,其右端出气管口放有脱脂棉。

(1)装置C中盛装的溶液是____________,D中试剂的作用是________。
(2)E中的红色布条是否退色?____,写出F中反应的化学反应方程式:____,其反应现象为_____________。
(3)新制氯水呈黄绿色说明其中含有_____,(填化学式,下同),将紫色石蕊溶液滴入可观察到的现象是_________________,说明其中含有__________。
(4)H中的试剂为___________,用来吸收多余氯气。工业上常用廉价的石灰乳吸收工业氯气尾气制得漂白精,该反应的化学方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是原子序数依次增大的短周期主族元素,三种元素原子序数之和为35,且C的原子序数是A的2倍。A、B、C三种元素的单质在适当条件下可发生如图所示的变化。下列说法正确的是

A. 甲、乙、丙三种物质的水溶液均显碱性
B. 甲是碱性氧化物,乙是酸性氧化物
C. 甲、乙可能都有漂白性,其漂白原理相同
D. 丙的水溶液在空气中长期放置,溶液可能会变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向Ba(OH)2和NaOH混合溶液中缓慢通入CO2至过量(溶液温度变化忽略不计),生成沉淀物质的量与通入CO2体积的关系如图所示。下列说法不正确的是
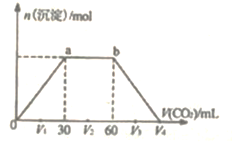
A. b点时溶质为NaHCO3
B. 横坐标轴上V4的值为90
C. oa过程是CO2与Ba(OH)2反应生成BaCO3的过程
D. 原混合物中 n[Ba(OH)2]:n(NaOH)=1:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
①标准状况下,6.02×1023个分子所占的体积约是22.4 L
②0.5 mol H2所占体积为11.2 L
③标准状况下,1 mol H2O的体积为22.4 L
④标准状况下,28 g CO与N2的混合气体的体积约为22.4 L
⑤各种气体的气体摩尔体积都约为22.4 L·mol-1
⑥标准状况下,体积相同的气体的分子数相同
A. ①③⑤B. ④⑥C. ②④⑥D. ①④⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com