
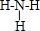 ,D2C含有的化学键类型为离子键;
,D2C含有的化学键类型为离子键; ;
;分析 A、B、C、D四种元素的原子序数均小于20,A元素所处的周期数、主族序数、原子序数均相等,则A为H元素;
B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3,则B为N元素;
C元素原子的最外层电子数比次外层少2个,则C是S元素;
C的阴离子与D的阳离子具有相同的电子层结构,两元素可形成化合物D2C,则D为K元素;
(1)A是H元素,C是S元素;
(2)主族元素原子核外电子层数等于其周期数、最外层电子数等于其族序数,据此判断B元素位置;
(3)A、B形成的化合物是氨气,K2S含有的化学键类型为离子键;
(4)K、S原子通过得失电子生成离子化合物硫化钾;
(5)A与D形成的化合物KH,KH和水反应生成KOH和氢气.
解答 解:A、B、C、D四种元素的原子序数均小于20,A元素所处的周期数、主族序数、原子序数均相等,则A为H元素;
B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3,则B为N元素;
C元素原子的最外层电子数比次外层少2个,则C是S元素;
C的阴离子与D的阳离子具有相同的电子层结构,两元素可形成化合物D2C,则D为K元素;
(1)A是H元素,C是S元素,故答案为:H;S;
(2)主族元素原子核外电子层数等于其周期数、最外层电子数等于其族序数,N原子核外有2个电子层、最外层电子数是5,所以位于第二周期第VA族,故答案为:第二周期第VA族;
(3)A、B形成的化合物是氨气,其结构式为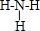 ,K2S含有的化学键类型为离子键,
,K2S含有的化学键类型为离子键,
故答案为: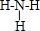 ;离子键;
;离子键;
(4)K、S原子通过得失电子生成离子化合物硫化钾, ,
,
故答案为: ;
;
(5)A与D形成的化合物KH,KH和水反应生成KOH和氢气,溶液中的溶质是KOH,溶液呈碱性,故答案为:碱.
点评 本题考查位置结构性质相互关系及应用,为高频考点,侧重考查元素推断、物质结构、物质性质、元素周期表等知识点,难点是用电子式表示物质形成过程.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | IVA族元素氢化物沸点顺序是:GeH4>SiH4>CH4;则VA族元素氢化物沸点顺序也是:AsH3>PH3>NH3 | |
| B. | 第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3;则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 | |
| C. | Fe3O4可以写成FeO•Fe2O3;Pb3O4也可以写成PbO•Pb2O3 | |
| D. | NaHSO4与NaHSO3溶于水显酸性,则所有酸式盐溶于水显酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化铝、碳酸钠都是常见的胃酸中和剂 | |
| B. | 红葡萄酒密封储存时间越长质量越好原因之一是生成了有香味的酯 | |
| C. | 碘酒中的碘因有还原性而起到杀菌消毒作用 | |
| D. | 食盐、食醋、味精是常用的食品添加剂,其主要成分均属于钠盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应 | |
| B. |  是同系物 是同系物 | |
| C. | 苯、乙烯都能使溴水褪色,但其原理不同 | |
| D. |  互为同分异构体 互为同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水与碳酸氢钠不反应 | |
| B. | 25℃时,0.1mol/L的醋酸溶液与0.01mol/L的醋酸溶液中,Ka前者小于后者 | |
| C. | NaClO溶液中通入少量二氧化碳的反应为:2NaClO+CO2+H2O=Na2CO3+2HClO | |
| D. | 等物质的量浓度的碳酸钠溶液、醋酸钠溶液、次氯酸钠溶液的pH pH(Na2CO3)>pH(NaClO)>pH(CH3COONa) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | WX2分子中所有原子最外层都为8电子结构 | |
| B. | WX2、ZX2均为酸性氧化物 | |
| C. | WX2是以极性键结合成的非极性分子 | |
| D. | 最简单氢化物的稳定性:W>X |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在酯水解试验中,可以通过观察酯层消失的时间差异,来判断乙酸乙酯在不同条件下水解速率的差别 | |
| B. | 探究“温度影响硫代硫酸钠与稀硫酸反应速率的因素”的实验中,需要用到的计量仪器只需量筒、温度计 | |
| C. | 在溴富集过程中,可在分液漏斗中加入4mL溴水,再向其中加入10mL四氯化碳,振荡,静置、分液,得下层液体 | |
| D. | 实验室制备乙烯常用硫酸铜溶液洗气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com