
| A. | SO2+2NaOH=Na2SO3+H2O | B. | SO2+Cl2+2H2O=H2SO4+2HCl | ||
| C. | SO2+2H2S=3S↓+2H2O | D. | SO2+NO2=SO3+NO |
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 根据分散系的稳定性将其分为胶体、溶液和浊液 | |
| B. | 根据化合物在溶液中能否电离将其分为强电解质和弱电解质 | |
| C. | 根据酸分子中含有的氢原子个数将酸分为一元酸、二元酸和多元酸 | |
| D. | 根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某实验小组设计了如图所示的甲醇燃料电池装置.
某实验小组设计了如图所示的甲醇燃料电池装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ②③④ | C. | ②④⑤ | D. | ①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
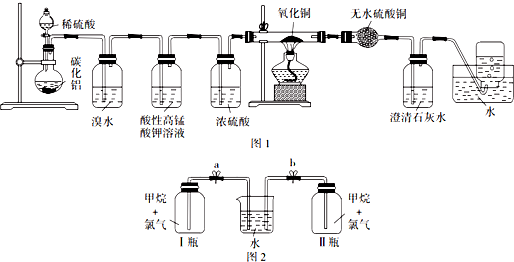
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
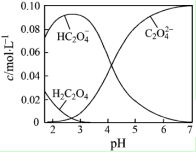 H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )
H2C2O4为二元弱酸.20℃时,配制一组c(H2C2O4)+c(HC2O4-)+c(C2O42-)=0.100mol•L-1的H2C2O4和NaOH混合溶液,溶液中部分微粒的物质的量浓度随pH的变化曲线如图所示.下列指定溶液中微粒的物质的量浓度关系一定正确的是( )| A. | pH=2.5的溶液中:c(H2C2O4)+c(C2O42-)>c(HC2O4-) | |
| B. | c(Na+)=0.100 mol•L-1的溶液中:c(H+)+c(H2C2O4)=c(OH-)+c(C2O42-) | |
| C. | c(HC2O4-)=c(C2O42-)的溶液中:c(Na+)>0.100 mol•L-1+c(HC2O4-) | |
| D. | pH=7的溶液中:c(Na+)>2c(C2O42-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将经过无害化处理的生活污水排放到漓江中 | |
| B. | 漓江沿岸不得开设造纸厂等污染企业 | |
| C. | 定期投放水生动物优化漓江生态 | |
| D. | 使用含磷洗涤剂且将洗涤后的废水排放到漓江中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com