
【题目】(1)写出醋酸的电离方程式:_____________________________________;
(2)写出醋酸电离平衡常数表达式:_______________;
(3)向0.1mol/L 醋酸溶液中加入水,电离平衡向_______移动 (填“左”或“右”) ;n(CH3COOH)_______; c(CH3COO-)/c(H+)_______(填“增大”、“减小”或“不变”);
(4)500mL 0.1mol/L 醋酸溶液a和500mL 0.1mol/L 盐酸溶液b与足量Zn粉反应,初始速率a___b;生成H2的量a____b;完全中和这两种酸,消耗NaOH的量a___b(填“<”、“>”或“=”)。
【答案】CH3COOH ![]() CH3COO-+H+
CH3COO-+H+ 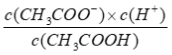 右 增大 减小 不变 = =
右 增大 减小 不变 = =
【解析】
(1)本题考查弱电解质的电离,醋酸属于弱酸,发生部分电离,电离方程式为CH3COOH ![]() CH3COO-+H+;(2)考查电离平衡常数,根据电离平衡常数的定义,醋酸的电离平衡常数为Ka=
CH3COO-+H+;(2)考查电离平衡常数,根据电离平衡常数的定义,醋酸的电离平衡常数为Ka= 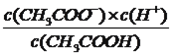 ;(3)考查影响电离平衡移动的因素,加水促进电离,电离平衡向右移动,n(CH3COOH)的减小,因为是同一溶液,c(CH3COO-)/c(H+)=n(CH3COO-)/n(H+),根据醋酸电离方程式,因此c(CH3COO-)/c(H+)不变;(4)本题考查一元强酸和一元强碱,醋酸是弱酸,盐酸是强酸,相同浓度时醋酸中c(H+)小于盐酸中c(H+),因此初始速率时a<b;锌是过量,盐酸和醋酸物质的量相同,因此产生氢气的量相同,即a=b;两种酸的物质的量相同,即消耗NaOH的量相等,即a=b。
;(3)考查影响电离平衡移动的因素,加水促进电离,电离平衡向右移动,n(CH3COOH)的减小,因为是同一溶液,c(CH3COO-)/c(H+)=n(CH3COO-)/n(H+),根据醋酸电离方程式,因此c(CH3COO-)/c(H+)不变;(4)本题考查一元强酸和一元强碱,醋酸是弱酸,盐酸是强酸,相同浓度时醋酸中c(H+)小于盐酸中c(H+),因此初始速率时a<b;锌是过量,盐酸和醋酸物质的量相同,因此产生氢气的量相同,即a=b;两种酸的物质的量相同,即消耗NaOH的量相等,即a=b。


科目:高中化学 来源: 题型:
【题目】铁镁合金是目前已发现的储氢密度较高的储氢材料之一,其晶胞结构如图所示(黑球代表Fe,白球代表Mg)。则下列说法不正确的是( )
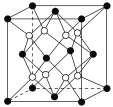
A. 铁镁合金的化学式为Mg2Fe
B. 晶体中存在的化学键类型为金属键
C. 晶格能:氧化钙>氧化镁
D. 该晶胞的质量是![]() g(NA表示阿伏加德罗常数的值)
g(NA表示阿伏加德罗常数的值)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)![]() pC(g) △H<0,在一定温度下,平衡时B的体积分数与压强变化的关系如图所示,则下列叙述正确的是( )
pC(g) △H<0,在一定温度下,平衡时B的体积分数与压强变化的关系如图所示,则下列叙述正确的是( )

①m+n<p ②x点的状态是v正>v逆 ③n>p ④x点比y点的反应速度慢 ⑤若升高温度,该反应的平衡常数增大
A. ①②④ B. ②④
C. ③⑤ D. ①③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物M(C16H14O2)是一种香料,工业上利用烃A和甲苯为主要原料,按下列路线合成:
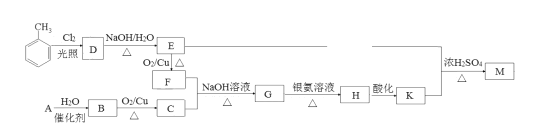
已知:①气态烃A在标准状况下的密度是1.25g/L;
②醛在碱性溶液中能发生羟醛缩合反应,再脱水生成不饱和醛:
RCH2-CHO+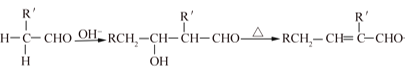 +H2O
+H2O
请回答下列问题:
(1)F的名称是____;G中含有的官能团名称是____。
(2)写出D→E的化学方程式___。
(3)A→B的反应类型是___;M的结构简式是____。
(4)同时满足下列条件的K的同分异构体有___种(不考虑立体异构)。
①遇FeCl3溶液发生显色反应②能发生银镜反应③除苯环以外不再含有其他环状结构
其中核磁共振氢谱为五组峰的结构简式为___。
(5)以乙醇为起始原料,选用必要的无机试剂合成1-丁烯,写出合成路线(用结构简式表示有机物),用箭头表示转化关系,箭头上注明试剂和反应条件)。___
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:
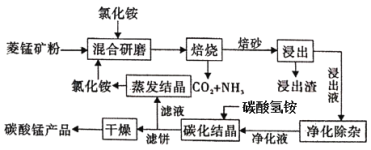
已知:①菱锰矿石主要成分是MnCO3,还含有少量Fe、Al、Ca、Mg等元素;
②常温下,CaF2、MgF2的溶度积分别为1.46×10-10、7.42×10-11
③相关金属离子c(Mn+)=0.1mol/L形成氯氧化物沉淀时的pH如下:
回答下列问题:
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
(1)“焙烧”时发生的主要化学反应方程式为______________________。
(2)分析下列图1、图2、图3,氯化铵焙烧菱镁矿的最佳条件是:
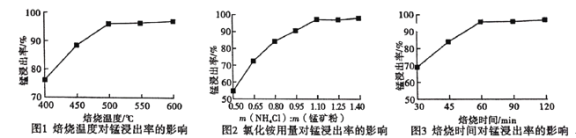
焙烧温度_________,氯化铵与菱镁矿粉的质量之比为__________,焙烧时间为___________.
(3)浸出液“净化除杂”过程如下:首先加入MnO2将Fe2+氧化为Fe3+,反应的离子方程式为________;然后调节溶液pH使Fe3+、Al3+沉淀完全,此时溶液的pH范围为____。再加入NH4F沉淀Ca2+、Mg2+,当c(Ca2+)=1.0×10-5mol/L时, c(Mg2+)=______mol/L
(4)碳化结晶时,发生反应的离子方程式为_____________________________________________。
(5)流程中能循环利用的固态物质是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一稀硫酸和稀硝酸的混合酸,其中H2SO4和HNO3的物质的量浓度分别是4mol/L和2mol/L,取10mL此混合酸,向其中加入过量的铁粉,待反应结束后,可产生标准状况下气体的体积为(设反应中HNO3被还原成NO)( )
A. 0.448LB. 0.672LC. 0.896LD. 0.224L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C、D四种短周期主族元素,A分别与B、C、D结合生成甲、乙、丙三种化合物,且甲、乙、丙三分子均为10电子粒子,C、D结合生成化合物丁。有关元素的单质和甲、乙、丙、丁四种化合物的转化关系如图所示。
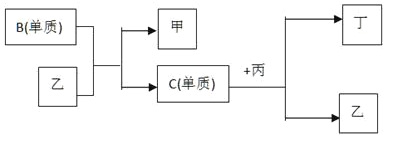
(1)根据以上条件可以确定A、B、C、D四种元素中的三种元素。不能被确定的第四种元素是____(填A、B、C、D中的一种)。
(2)依据下列条件可以进一步确定上述第四种元素:①甲与丙以及乙与丙均能够发生反应;②甲、丙都是无色、有刺激性气味的物质。据此,写出C+丙=乙+丁的化学方程式:___________。
(3)NH3H2O的电离方程式为NH3H2O![]() NH4++OH-,试判断NH3溶于水后形成的NH3H2O的合理结构 ________(填字母代号)。
NH4++OH-,试判断NH3溶于水后形成的NH3H2O的合理结构 ________(填字母代号)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制备溴苯可用下图所示装置。请回答下列问题
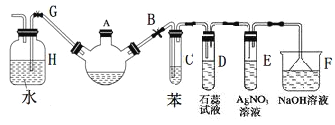
(1)关闭G夹,打开B夹,从装有少量苯的三颈烧瓶的A口加少量溴,再加入少量铁屑,塞住A口,三颈烧瓶中发生的主要反应的化学方程式为_________________________________。
(2)试管C中苯的作用是:____________________。试管D中出现的现象是:_____________。试管E中出现的现象是:___________________。
(3)待三颈烧瓶中的反应进行到仍有气泡冒出时打开G夹,关闭B夹,可以看到的现象是_______________ 。
(4)三颈烧瓶中的溴苯经过下列步骤分离提纯:
①向三颈烧瓶中加入10 mL水,然后过滤除去未反应的铁屑;
②滤液依次用10 mL水、8 mL10%的NaOH溶液、10 mL水洗涤。NaOH溶液洗涤的作用是__________;
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤。加入氯化钙的目的是_______。
④经过上述分离操作后,要进一步提纯,下列操作中必须的是_______(填入正确选项前的字母):
A.重结晶 B.过滤 C.蒸馏 D.萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应:![]() (Q>0),达到平衡后,改变一个条件,以下有关分析正确的是
(Q>0),达到平衡后,改变一个条件,以下有关分析正确的是
A.升高温度,正反应速率增大,化学平衡常数增大
B.减小压强,逆反应速率减小,化学平衡常数减小
C.加入催化剂,正逆反应速率不变,平衡不移动
D.充入氧气,正反应速率先增大后减小,平衡向正反应方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com