
分析 因活泼性Fe>Cu,将Fe和Cu的混合粉末加入FeCl3溶液中,可先后发生2FeCl3+Fe=3FeCl2、2FeCl3+Cu=2FeCl2+CuCl2,以此解答该题.
解答 解:(1)若反应后只有Cu剩余,可Fe完全反应,一定发生2FeCl3+Fe=3FeCl2,可能发生2FeCl3+Cu=2FeCl2+CuCl2,则溶液中阳离子一定有Fe2+,可能有Cu2+,故答案为:Fe2+;Cu2+;
(2)若反应后有Fe剩余,则只发生2FeCl3+Fe=3FeCl2,溶液中阳离子一定有Fe2+,一定没有Fe3+、Cu2+,故答案为:Fe2+;Fe3+、Cu2+.
点评 本题考查元素元素化合物知识,侧重Fe3+、Cu2+的氧化能力大小的比较,为高频考点,能正确判断固体的成分是解本题的关键,根据固体的成分了解反应的先后顺序,从而确定溶液的成分,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 原溶液中投入铁粉物质的量是0.5mol | |
| B. | 原溶液中的HNO3浓度是2.0mol•L-1 | |
| C. | 反应后的溶液中c(Fe2+):c(Fe3+)=1:1 | |
| D. | 反应后的溶液中还可以溶解16.0g铜 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
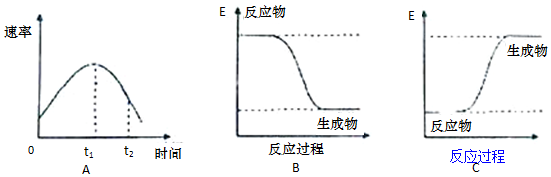
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 晶体熔点的高低: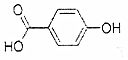 > >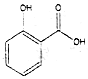 | |
| B. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| C. | 熔点由高到低:Na>Mg>Al | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
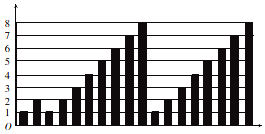
| A. | 横坐标为质子数,纵坐标为元素的最高正价 | |
| B. | 横坐标为原子序数,纵坐标为元素原子的最外层电子数 | |
| C. | 横坐标为核电荷数,纵坐标为元素原子的半径 | |
| D. | 横坐标为中子数,纵坐标为元素的非金属性 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 化学反应速率是化学反应进行快慢程度的物理量 | |
| B. | 化学反应速率的常用单位有mol/(L•s)和mol/(L•min) | |
| C. | 在同一个反应中,可以用反应物或生成物来表示反应速率 | |
| D. | 化学反应速率通常用单位时间内生成或消耗某物质的质量的多少来表示 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
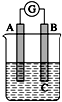 如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )| A. | A是Zn,B是Cu,C为稀硫酸 | B. | A是Cu,B是Zn,C为稀硫酸 | ||
| C. | A是Fe,B是Ag,C为稀AgNO3溶液 | D. | A是Ag,B是Fe,C为稀AgNO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com