
 为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为0.1mol/L KMnO4标准溶液滴定.
为测定某H2C2O4溶液的浓度,取该溶液于锥形瓶中,加入适量稀H2SO4后,用浓度为0.1mol/L KMnO4标准溶液滴定.| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗KMnO4溶液体积/mL | 30.32 | 25.34 | 25.30 |
分析 (1)KMnO4具有强氧化性,会腐蚀橡胶管;滴定终点时溶液颜色无色变化为紫色且在30s内颜色不再恢复为原来颜色,证明反应达到终点;
(2)A与C刻度间相差1ml,说明每两个小格之间是0.1mL,A处的刻度21,据此确定B的刻度,注意滴定管的上面数值小,下面数值大;
(3)根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$判断不当操作对相关物理量的影响;
(4)根据离子方程式6H++2MnO4-+5H2C2O4═2Mn2++10CO2↑+8H2O计算H2C2O4的浓度.
解答 解:(1)因为KMnO4具有强氧化性,会腐蚀橡胶管,故应用酸式滴定管盛装;KMnO4溶液呈紫色,草酸反应完毕,当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色,即达滴定终点;
故答案为:酸式;当滴入最后一滴KMnO4溶液时,溶液由无色变为紫色,且半分钟内不褪色;
(2)A与C刻度间相差1ml,说明每两个小格之间是0.10mL,A处的刻度为21,A和B之间是四个小格,所以相差0.40mL,则B是21.40mL;
故答案为:21.40;
(3)①实验结束时俯视刻度线读取滴定终点时KMnO4溶液的体积,液面偏高,读数偏小,导致KMnO4体积偏小,则根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$使结果偏低,故正确;
②酸式滴定管未用标准液润洗,KMnO4浓度偏小,导致KMnO4体积偏大,则根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$使结果偏高,故错误;
③锥形瓶用待测液润洗,导致草酸的物质的量偏大,导致KMnO4体积偏大,则根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$使结果偏高,故错误
④滴加KMnO4溶液过快,未充分振荡,刚看到溶液变色,立刻停止滴定,导致KMnO4体积偏小,则根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$使结果偏低,故正确;
故选:①④;
(4)三次滴定消耗KMnO4溶液体积分别为:30.32mL、25.34mL、25.30mL,第一次误差较大,舍去,则消耗KMnO4溶液平均体积为$\frac{25.34mL+25.30mL}{2}$=25.32ml,消耗KMnO4物质的量为n(KMnO4)=0.1mol/L×25.32×10-3L=2.532×10-3mol,由6H++2MnO4-+5H2C2O4═2Mn2++10CO2↑+8H2O可知,n(H2C2O4)=$\frac{5}{2}$n(KMnO4)=$\frac{5}{2}$×2.532×10-3mol,则H2C2O4的物质的量浓度C=$\frac{\frac{5}{2}×2.532×10{\;}^{-3}mol}{0.03L}$=0.211mol/L;
故答案为:0.211.
点评 本题主要考查氧化还原反应滴定、化学计算等,难度中等,清楚实验原理是解题的关键,需要学生具备扎实的基础知识与综合运用知识分析问题、解决问题的能力.


科目:高中化学 来源: 题型:选择题
| A. | 可溶性铁盐或铝盐可用于水的净化 | |
| B. | 电解MgCl2溶液可制得金属镁 | |
| C. | 在海轮的外壳镶上锌块,可减缓船体的腐蚀速率 | |
| D. | “开发利用新能源”、“汽车尾气催化净化”都能提高空气质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
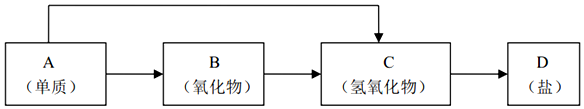
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 | 8 | … | 16 | 18 |
| n(X)/mol | 1.600 | 1.200 | 1.100 | 1.075 | … | … | 1.000 | 1.000 |
| A. | 4-6 min时间段内Z的平均反应速率2.5×10-3 mol/(L•min) | |
| B. | 该温度下此反应的平衡常数K=1.44 | |
| C. | 达平衡后,升高温度,K减小,则正反应△H>0 | |
| D. | 其他条件不变,再充入1.6 mol Z,达新平衡时Z的体积分数不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 中子数为18的硫原子:${\;}_{16}^{34}S$ | B. | 次氯酸的结构式:H-Cl-O | ||
| C. | H2O2的电子式: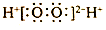 | D. | 乙烯的结构简式:CH2CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
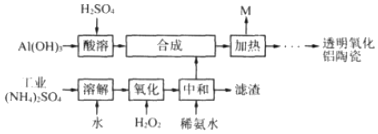
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com