
| Y | ||
| X | ||
| Z |
| A. | Y是非金属性最强的元素 | B. | Z是金属元素 | ||
| C. | Y的原子序数为a-7 | D. | X的气态氢化物化学式为H2X |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:多选题
| A. | 甲和乙中反应的化学平衡常数相同 | |
| B. | 乙和丙中的二氧化硫的生成速率相同 | |
| C. | 乙中SO3的体积分数大于丙 | |
| D. | 转化率:α甲(SO2)+α乙(SO3)<1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
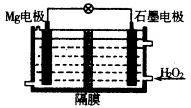 钠、镁、铁、铜及其化合物在科研和生产生活中有广泛的应用.
钠、镁、铁、铜及其化合物在科研和生产生活中有广泛的应用.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 其含有的共价键类型是极性共价键.
其含有的共价键类型是极性共价键.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将溶液稀释到原体积的10倍 | B. | 加入适量的醋酸钠固体 | ||
| C. | 加入等体积0.1 mol/L烧碱溶液 | D. | 加入等体积0.1 mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3+、Br-、Al3+、H+、CO32-、H2PO4-这些离子都能破坏水的电离平衡 | |
| B. | 常温下,往饱和石灰水中加入一定量的生石灰,一段时间后恢复到原温度,溶液的pH变小 | |
| C. | CuSO4、K2CO3、KMnO4的水溶液分别在空气中小心加热蒸干至质量不再减少为止,都能得到较纯净的原溶质 | |
| D. | Na2C2O4溶液中存在:c(OH-)=c(H+)+c(H2C2O4) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
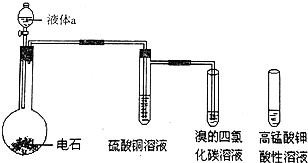 如图是实验室制取乙炔气体及乙炔的性质实验的装置,气密性已检验,部分夹持装置略.
如图是实验室制取乙炔气体及乙炔的性质实验的装置,气密性已检验,部分夹持装置略. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com