

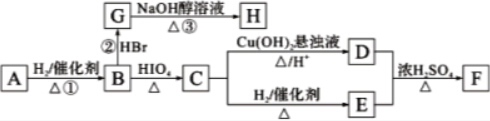
分析 烃A的密度是相同条件下氢气密度的14倍,应为28,则A为CH2=CH2,A与水在催化剂作用下生成B为CH3CH2OH,A与溴发生加成生成C为CH2BrCH2Br,C在碱性条件下水解得D为CH2OHCH2OH,D与氧气发生氧化得E为OHCCHO,E氧化得F为HOOCCOOH,B与F发生酯化反应得G为CH3COOCH2CH2OOCCH3,A发生氧化反应得H为CH3CHO,H氧化得I为CH3COOH,D与I发生酯化反应得J为CH3COOCH2CH2OOCCH3,据此答题.
解答 解:烃A的密度是相同条件下氢气密度的14倍,应为28,则A为CH2=CH2,A与水在催化剂作用下生成B为CH3CH2OH,A与溴发生加成生成C为CH2BrCH2Br,C在碱性条件下水解得D为CH2OHCH2OH,D与氧气发生氧化得E为OHCCHO,E氧化得F为HOOCCOOH,B与F发生酯化反应得G为CH3CH2OOC-COOCH2CH3,A发生氧化反应得H为CH3CHO,H氧化得I为CH3COOH,D与I发生酯化反应得J为CH3COOCH2CH2OOCCH3,
(1)根据上面的分析可知,A为CH2=CH2,A的化学式是C2H4,G的结构简式为CH3CH2OOC-COOCH2CH3,
故答案为:C2H4;CH3CH2OOC-COOCH2CH3;
(2)根据上面的分析可知,在A-J的各种物质中,属于醇类是B、D,属于醛类的是E、H,
故答案为:B、D;E、H;
(3)C→D的化学方程式为CH2BrCH2Br+2H2O$→_{△}^{NaOH}$CH2OHCH2OH+2HBr,D+I→J的化学方程式为2CH3COOH+HOCH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$ CH3COOCH2CH2OOCCH3+2H2O,A $\stackrel{O_{2}}{→}$H的化学方程式为2CH2=CH2+O2 $\stackrel{催化剂}{→}$ 2CH3CHO,
故答案为:2CH3COOH+HOCH2CH2OH$→_{△}^{浓H_{2}SO_{4}}$ CH3COOCH2CH2OOCCH3+2H2O;2CH2=CH2+O2 $\stackrel{催化剂}{→}$ 2CH3CHO.
点评 本题考查有机物的推断,题目难度不大,本题注意以A为解答该题的突破口,根据有机物反应的条件判断可能进行的反应,注意把握有机物官能团的性质,为解答该类题目的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
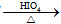 RCHO+R′CHO
RCHO+R′CHO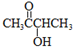 .
. CH3COO-+NH4++2Ag↓+3NH3+H2O.
CH3COO-+NH4++2Ag↓+3NH3+H2O. .若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为
.若H分子中所有碳原子均在一条直线上,则G转化为H的化学方程式为 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
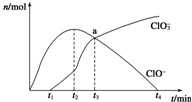 工业上把Cl2通入NaOH溶液中制得漂白液(主要成分NaClO).一化学小组模拟实验得到ClO-、ClO${\;}_{3}^{-}$等离子其物质的量(mol)与反应时间t(min)的关系曲线:
工业上把Cl2通入NaOH溶液中制得漂白液(主要成分NaClO).一化学小组模拟实验得到ClO-、ClO${\;}_{3}^{-}$等离子其物质的量(mol)与反应时间t(min)的关系曲线:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同质量的N2和CO2 | B. | 同质量的H2和N2 | ||
| C. | 同体积的O2和N2 | D. | 相同物质的量的N2O和CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AlON和石英的化学键类型相同 | |
| B. | AlON和石英晶体类型相同 | |
| C. | AlON中N元素的化合价为-1 | |
| D. | 电解熔融AlON或电解熔融Al2O3都能得到Al |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图表示一个电解池,装有电解质溶液a,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解质溶液a,X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.
科学家把C60和钾掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用水润湿的pH试纸来测量溶液的pH | |
| B. | 实验需要480mL 2.0mol•L-1的氢氧化钠溶液.配制该溶液时先称量氢氧化钠固体38.4g,然后再按照溶解、冷却、移液、洗涤、定容、摇匀的步骤进行操作 | |
| C. | 向溶液中滴加硝酸酸化的Ba(NO3)2溶液出现白色沉淀,说明溶液中一定有SO42- | |
| D. | 用溴水,淀粉、KI溶液比较Br2与I2的氧化性强弱,所需玻璃仪器主要有:试管、胶头滴管 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com