
分析 (1)工业生产硅的原理为:2C+SiO2═Si+2CO↑;
(2)氢氧化亚铁、氧气、水反应生成氢氧化铁;
(3)金属钠与硫酸铜溶液反应,钠性质活泼,钠先和水剧烈反应生成NaOH和氢气,为氧化还原反应,NaOH与硫酸铜反应生成氢氧化铜和硫酸钠,据此分析解答;
(4)实验室用氯化铵和碱石灰反应制取氨气,据此进行回答;
解答 解:(1)工业生产硅的原理为:2C+SiO2═Si+2CO↑,
故答案为:2C+SiO2═Si+2CO↑;
(2)氢氧化亚铁、氧气、水反应生成氢氧化铁,方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
故答案为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
(3)钠先和水反应为氧化还原反应,氧化剂H2O,被氧化的元素Na,氧化产物NaOH,生成NaOH和氢气,反应的化学方程式为:2Na+2H2O=2NaOH+H2↑,离子反应为2Na+2H2O═2Na++2OH-+H2↑,NaOH与硫酸铜发生复分解反应,反应的化学方程式为CuSO4+2NaOH═Cu(OH)2↓+Na2SO4,生成氢氧化铜和硫酸钠,离子反应为Cu2++2OH-=Cu(OH)2↓,总反应为:2Na+Cu2++2H2O=2Na++Cu(OH)2↓+H2↑,故答案为:2Na+Cu2++2H2O=2Na++Cu(OH)2↓+H2↑;
(4)实验室用氯化铵和碱石灰反应制取氨气,即碱与盐反应生成新碱和新盐,化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$Ca Cl2+2NH3↑+2H2O;
点评 本题主要考查了方程式的书写,难度不大,根据所学知识即可完成.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 10℃时,20mL3mol/L的X溶液 | B. | 20℃时,30mL2mol/L的X溶液 | ||
| C. | 20℃时,20mL4mol/L的X溶液 | D. | 10℃时,10mL2mol/L的X溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇 | B. | 三氯乙烯 | C. | 乙酸 | D. | 甘油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+ MnO4- NO3-Na+ | B. | Na+NH4+Ba2+K+ | ||
| C. | Na+SO32-SO42-K+ | D. | K+Ca2+NO3-K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
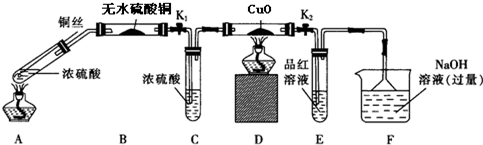
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com