
”¾ĢāÄæ”潫1 mol I2(g)ŗĶ2 mol H2ÖĆÓŚ2LĆܱÕČŻĘ÷ÖŠ£¬ŌŚŅ»¶ØĪĀ¶ČĻĀ·¢Éś·“Ó¦£ŗI2(g) + H2(g) ![]() 2HI(g)£»”÷H£¼0£¬²¢“ļĘ½ŗā”£HIµÄĢå»ż·ÖŹżw(HI)Ėꏱ¼ä±ä»ÆČēĶ¼ĒśĻß(¢ņ)ĖłŹ¾£ŗ
2HI(g)£»”÷H£¼0£¬²¢“ļĘ½ŗā”£HIµÄĢå»ż·ÖŹżw(HI)Ėꏱ¼ä±ä»ÆČēĶ¼ĒśĻß(¢ņ)ĖłŹ¾£ŗ
£Ø1£©“ļĘ½ŗāŹ±£¬I2(g)µÄĪļÖŹµÄĮæÅضČĪŖ____________________”£
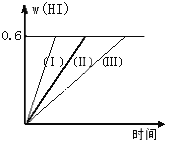
£Ø2£©Čōøı䷓ӦĢõ¼ž£¬ŌŚ¼×Ģõ¼žĻĀw(HI)µÄ±ä»ÆČēĒśĻß(¢ń)ĖłŹ¾£¬ŌŚŅŅĢõ¼žĻĀw(HI)µÄ±ä»ÆČēĒśĻß(¢ó) ĖłŹ¾”£Ōņ¼×Ģõ¼žæÉÄÜŹĒ____________£¬ŌņŅŅĢõ¼žæÉÄÜŹĒ_____________ ”££ØĢīČėĻĀĮŠĢõ¼žµÄŠņŗÅ£©
¢ŁŗćČŻĢõ¼žĻĀ£¬ÉżøßĪĀ¶Č£»¢ŚŗćČŻĢõ¼žĻĀ£¬½µµĶĪĀ¶Č£»¢ŪŗćĪĀĢõ¼žĻĀ£¬ĖõŠ”·“ӦȯĘ÷Ģå»ż£»
¢ÜŗćĪĀĢõ¼žĻĀ£¬Ą©“ó·“ӦȯĘ÷Ģå»ż£»¢ŻŗćĪĀŗćČŻĢõ¼žĻĀ£¬¼ÓČėŹŹµ±“߻ƼĮ”£
£Ø3£©Čō±£³ÖĪĀ¶Č²»±ä£¬ŌŚĮķŅ»øöĻąĶ¬µÄ2LĆܱÕČŻĘ÷ÖŠ¼ÓČėa mol I2(g)”¢b mol H2(g)ŗĶc mol HI£Øa”¢b”¢c¾ł“óÓŚ0£©£¬·¢Éś·“Ó¦£¬“ļĘ½ŗāŹ±£¬HIµÄĢå»ż·ÖŹżČŌĪŖ0.6£¬Ōņa”¢b”¢cµÄ¹ŲĻµŹĒ____________”£
”¾“š°ø”æ 0.05mol”¤L£1 ¢Ū¢Ż ¢Ü (a£«c/2)/(b£«c/2)=1/2
”¾½āĪö”æŹŌĢā·ÖĪö£ŗ£Ø1£©øĆ·“Ó¦ŹĒŅ»øö·“Ó¦Ē°ŗóĘųĢåĢå»ż²»±äµÄ»Æѧ·“Ó¦£¬ĖłŅŌ·“Ó¦ŗó»ģŗĻĘųĢåµÄĪļÖŹµÄĮæŹĒ3mol£¬Ķ¬Ņ»ČŻĘ÷ÖŠø÷ÖÖĘųĢåµÄĢå»ż·ÖŹżµČĘäĪļÖŹµÄĮæ·ÖŹż£¬ĖłŅŌĘ½ŗāŹ±µā»ÆĒāµÄĪļÖŹµÄĮæ=3mol”Į0.6=1.8mol£¬Ōņ²Ī¼Ó·“Ó¦µÄn£ØI2£©=0.5n£ØHI£©=0.5”Į1.8=0.9mol£¬Ź£ÓąµÄn£ØH2£©=1-0.9=0.1mol£¬ĖłŅŌĘ½ŗāŹ±c£ØH2£©=![]() =0.05mol/L£¬¹Ź“š°øĪŖ£ŗ0.05mol/L£»
=0.05mol/L£¬¹Ź“š°øĪŖ£ŗ0.05mol/L£»
£Ø2£©ŌŚ¼×Ģõ¼žĻĀw£ØHI£©µÄ±ä»ÆČēĒśĻߣآń£© ĖłŹ¾£¬·“Ó¦Ź±¼äĖõ¶Ģ£¬µā»ÆĒāµÄŗ¬Įæ²»±ä£¬ĖµĆ÷øĆĢõ¼žÖ»Ōö“óĮĖ·“Ó¦ĖŁĀŹ²»Ó°ĻģĘ½ŗā£¬Ōö“óŃ¹Ēæ£ØĖõŠ”·“ӦȯĘ÷Ģå»ż£©ŗĶ¼ÓČė“߻ƼĮ¶ŌøĆ·“Ó¦Ę½ŗāĪŽÓ°Ļģ£¬µ«¶¼Ōö“ó·“Ó¦ĖŁĀŹ£¬Ėõ¶Ģ·“Ó¦Ź±¼ä£»ŌŚŅŅĢõ¼žĻĀw£ØHI£©µÄ±ä»ÆČēĒśĻß£Ø¢ó£© ĖłŹ¾£¬·“Ó¦Ź±¼ä±ä³¤£¬µā»ÆĒāµÄŗ¬Įæ²»±ä£¬ĖµĆ÷·“Ó¦ĖŁĀŹ¼õŠ”£¬Ę½ŗā²»ŅĘ¶Æ£¬ĖłŅŌŹĒ¼õŠ”Ń¹Ēæ£ØĄ©“óČŻĘ÷Ģå»ż£©£¬¹Ź“š°øĪŖ£ŗ¢Ū¢Ż£»¢Ü£»
£Ø3£©Čō±£³ÖĪĀ¶Č²»±ä£¬ŌŚĮķŅ»øöĻąĶ¬µÄ2LĆܱÕČŻĘ÷ÖŠ¼ÓČėa mol I2£Øg£©”¢b mol H2£Øg£©ŗĶc mol HI£Øa”¢b”¢c¾ł“óÓŚ0£©£¬·¢Éś·“Ó¦£¬“ļĘ½ŗāŹ±£¬HIµÄĢå»ż·ÖŹżČŌĪŖ0.6£¬ÓėŌĄ“µÄĘ½ŗāŹĒµČŠ§Ę½ŗā£¬ŗćĪĀŗćČŻ£¬Ē°ŗóĘųĢåĢå»ż²»±ä»Æ£¬°“»Æѧ¼ĘĮæŹż×Ŗ»Æµ½×ó±ß£¬Āś×ćÓėŌĄ“¼ÓČėµÄ·“Ó¦ĪļĪļÖŹµÄĮæ±ČĄżĻąµČ¼“æÉ£»
I2£Øg£© + H2£Øg£©![]() 2HI£Øg£©£»
2HI£Øg£©£»
æŖŹ¼£Ømol£©£ŗa b c
±ä»Æ£Ømol£©£ŗ0.5c 0.5c c
Ę½ŗā£Ømol£©£ŗa+0.5c b+0.5c 0
Ōņ£Øa+0.5c £©£ŗ£Ø b+0.5c£©=1£ŗ2£¬ĖłŅŌ4a+c=2b£¬¹Ź“š°øĪŖ£ŗ4a+c=2b”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻņFe 2 (SO 4 ) 3 ŗĶAl 2 (SO 4 ) 3 µÄ»ģŗĻČÜŅŗÖŠ£¬ÖšµĪ¼ÓČėNaOHČÜŅŗÖĮ¹żĮ攣ĻĀĮŠĶ¼ĻóÖŠ£¬ÄÜÕżČ·±ķŹ¾ÉĻŹö·“Ó¦µÄŹĒ

A. A B. B C. C D. D
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æH2ŌŚO2ÖŠČ¼ÉÕÉś³ÉĘųĢ¬H2OµÄ·“Ó¦ŹĒŅ»øö·ÅČČ·“Ó¦£¬ŌŚ·“Ó¦¹ż³ĢÖŠ
A. ŗĖÄÜ×Ŗ»Æ³ÉČČÄÜ B. »ÆѧÄÜ×Ŗ»Æ³ÉČČÄÜ
C. Éś³ÉĪļµÄ×ÜÄÜĮæµČÓŚ·“Ó¦ĪļµÄ×ÜÄÜĮæ D. Éś³ÉĪļµÄ×ÜÄÜĮæ“óÓŚ·“Ó¦ĪļµÄ×ÜÄÜĮæ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖĖ®µÄµēĄėĘ½ŗāĒśĻßČēĶ¼ĖłŹ¾£¬ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ

£Ø1£©Ķ¼ÖŠĪåµćkw¼äµÄ¹ŲĻµŹĒ_____________”£
£Ø2£©Čō“ÓAµćµ½Dµć£¬æɲÉÓƵēėŹ©ŹĒ ”£
a.ÉżĪĀ b.¼ÓČėÉŁĮæµÄŃĪĖį c.¼ÓČėÉŁĮæµÄNH4Cl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲŅĒĘ÷µÄŹ¹ÓĆÕżČ·µÄŹĒ£Ø£©
A. ŹÖ³ÖŹŌ¹ÜøųŹŌ¹ÜÄŚµÄĪļÖŹ¼ÓČČ
B. ÓĆČ¼×ÅµÄ¾Ę¾«µĘČ„µćČ¼ĮķŅ»Õµ¾Ę¾«µĘ
C. ÓĆĢģĘ½³ĘĮæŅ©Ę·Ź±ÓĆŹÖÖ±½ÓÄĆķĄĀė
D. ÓƵĪ¹ÜµĪ¼ÓŅŗĢåŹ±µĪ¹ÜÓ¦“¹Ö±Šü“¹ŌŚČŻĘ÷ÉĻ·½ĒŅ²»ÄÜ“„¼°ČŻĘ÷ÄŚ±Ś
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠŹµŃé²Ł×÷ÄÜ“ļµ½ŹµŃéÄæµÄµÄŹĒ
A. ÓĆÅÅĖ®·ØŹÕ¼ÆĶ·ŪÓėÅØĻõĖį·“Ó¦²śÉśµÄNO2
B. ÓĆ°±Ė®¼ų±šNaCl”¢MgCl2”¢AlCl3”¢NH4ClĖÄÖÖČÜŅŗ
C. ÓĆĖįŠŌKMnO4ČÜŅŗŃéÖ¤²ŻĖįµÄ»¹ŌŠŌ
D. ÓƱ„ŗĶNaHCO3ČÜŅŗ³żČ„Cl2ÖŠ»ģÓŠµÄHCl
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŃÖŖŌŚ1”Į105 Pa”¢298 KĢõ¼žĻĀ£¬2 molĒāĘųČ¼ÉÕÉś³ÉĖ®ÕōĘų£¬·Å³ö484 kJČČĮ棬ĻĀĮŠČČ»Æѧ·½³ĢŹ½ÕżČ·µÄŹĒ(”” ””)
A. H2O(g)===H2(g)£«![]() O2(g)””¦¤H£½£«242 kJ”¤mol£1
O2(g)””¦¤H£½£«242 kJ”¤mol£1
B. 2H2(g)£«O2(g)===2H2O(l)””¦¤H£½£484 kJ”¤mol£1
C. H2(g)£«![]() O2(g)===H2O(g)””¦¤H£½£«242 kJ”¤mol£1
O2(g)===H2O(g)””¦¤H£½£«242 kJ”¤mol£1
D. 2H2(g)£«O2(g)===2H2O(g)””¦¤H£½£«484 kJ”¤mol£1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¼ÓŃ¹½µĪĀæÉŅŌŹ¹æÕĘųŅŗ»Æ£¬ŌŚ“Ė¹ż³ĢÖŠ£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®æÕĘųÖŠµÄ·Ö×ÓÖŹĮæ±ä“ó B£®æÕĘųÖŠµÄ·Ö×Ó¼äøō±äŠ”
C£®æÕĘųÖŠµÄ·Ö×ÓÖÖĄąøıä D£®æÕĘųÖŠµÄ·Ö×ÓŹżÄæ±äÉŁ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÄÜÓĆĄÕɳĢŲĮŠŌĄķ½āŹĶµÄŹĒ£Ø £©
A£®Fe£ØSCN£©3ČÜŅŗÖŠ¼ÓČė¹ĢĢåKSCNŗóŃÕÉ«±äÉī
B£®×ŲŗģÉ«NO2¼ÓŃ¹ŗóŃÕÉ«ĻȱäÉīŗó±äĒ³
C£®SO2“ß»ÆŃõ»Æ³ÉSO3µÄ·“Ó¦£¬ĶłĶłŠčŅŖŹ¹ÓĆ“ß»Æ¼Į
D£®H2”¢I2”¢HIĘ½ŗā»ģŗĶĘų¼ÓŃ¹ŗóŃÕÉ«±äÉī
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com