
分析 (1)根据各元素的含量确定有机物中各原子的个数,进而确定有机物分子式;
(2)A在常温下A可与浓溴水反应,说明A物质属于酚类,1molA最多可与2molBr2作用,说明羟基和甲基处于邻位或对位.
解答 解:(1)已知:M(A)=108,则有:
N(C)=$\frac{108×77.8%}{12}$=7,
N(H)=$\frac{108×7.4%}{1}$=8,
N(O)=$\frac{108×(1-77.8%-7.4%)}{16}$=1,
所以,A的分子式为C7H8O,
答:有机物的分子式为C7H8O;
(2)A在常温下A可与浓溴水反应,说明A物质属于酚类,1molA最多可与2molBr2作用,说明羟基和甲基处于邻位或对位,则A的可能结构简式是: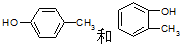 ,
,
答:该有机物的结构简式为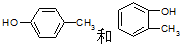 .
.
点评 本题考查有机物分子式的确定,为高频考点,侧重于学生的分析、计算能力的考查,题目难度不大,本题易错点为(2),注意苯酚与溴发生取代反应的性质.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | ②不对 | B. | ③不对 | C. | ①不对 | D. | 全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
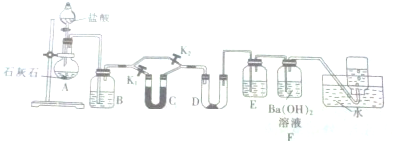
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
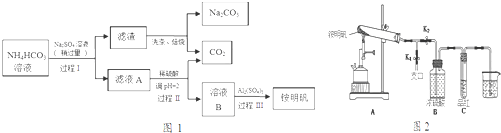
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
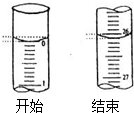 某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:
某校化学兴趣小组的同学对一含有少量Na2SO4的NaOH样品中NaOH的含量进行测定,请回答下列问题:| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol/L盐酸的体积(mL) | |
| 滴定前刻度 | 滴定后刻度 | ||
| 第一次 | 20.00 | 0.00 | 26.01 |
| 第二次 | 20.00 | 1.56 | 30.30 |
| 第三次 | 20.00 | 0.22 | 26.21 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
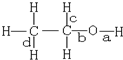
| A. | 和乙酸发生酯化反应键a断裂 | |
| B. | 和氢溴酸反应键a断裂 | |
| C. | 在铜催化和加热条件下和氧气反应键a、c断裂 | |
| D. | 和浓硫酸共热至170℃时键b和d断裂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铜 | B. | 铝 | C. | 铁 | D. | 钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| A2D | 187 | 202 | 2.6 |
| A2C2 | 272 | 423 | 以任意比互溶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com