
已知:25 ℃,Ksp [M(OH)2]=3.2×10-11,则此温度下M(OH)2饱和溶液的pH 等于
A.10 B.10+lg2
C.10+2×lg2 D.10-2×lg2
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案科目:高中化学 来源:2014-2015黑龙江省鸡西市龙东南四校高二上学期期末联考化学试卷(解析版) 题型:填空题
(11分) I:常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①、②、③的实验,实验数据记录如下表
序号 | HA物质的量浓度(mol·L-1) | NaOH物质的量浓度(mol·L-1) | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
请回答:
(1)根据①组实验情况,分析混合溶液的pH=9的原因是 (用反应的离子方程式表示),在该溶液中下列关系式不正确的是(填序号字母)________。
A.c(Na+)+c(H+)=c(OH-)+c(A-)
B.c(Na+)=c(HA)+c(A-)
C.c(HA)+c(H+)=c(OH-)
D.c(Na+)+c(H+)=c(OH-)+c(A-)+c(HA)
(2)②组情况表明,c 0.2mol·L-1。混合溶液中离子浓度c(A-) c(Na+)(选填“>”、“<”或“=”)
(3)从③组实验结果分析,说明HA的电离程度 NaA的水解程度(选填“>”、“<”或“=”),离子浓度由大到小的顺序是__________________________。
Ⅱ:室温下,若将0.1 mol·L-1盐酸滴入20 mL 0.1 mol·L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示。
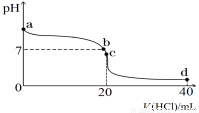
(1)NH3·H2O的电离方程式是 。
(2)b点所示溶液中的溶质是 。
(3)c点所示溶液中,离子浓度从大到小的关系为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省鸡西市龙东南七校高一上学期期末联考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是
A.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
C.三氯化铁溶液中加入铁粉:
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:填空题
(8分)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的1/4。
(1)为了降低某水库的铁闸门被腐蚀的速率,可以采用下图所示甲的方案,属于 原理(填“原电池”或“电解池”)
(2)下图中乙方案也可降低铁闸门腐蚀速率,称为 保护法。
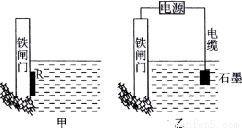
(3)将5 mol/L CuSO4溶液200mL用惰性电极电解一段时间后,从其中的一个电极收集到标准状况下448 mL气体,为使电解后的溶液恢复到开始的浓度,应向电解后的溶液中加入 g 物质(填化学式)。
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
常温下,0.2mol/L的一元酸HA与等浓度的NaOH溶液等体积混合后,所得溶液中部分微粒组分及浓度如下图所示,下列说法正确的是

A.HA为强酸
B.该混合液pH=7
C.图中X表示HA,Y表示OH—,Z表示H+
D.该混合溶液中:c(A—)+ c(Y)=c(Na+)
查看答案和解析>>
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:选择题
将2molSO2和2molSO3气体,混合于一固定体积的密闭容器中,在一定条件下发生反应:2SO2+O2 2SO3平衡时SO3为W mol;在相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,平衡时SO3的物质的量大于W mol的是
2SO3平衡时SO3为W mol;在相同温度下,分别按下列配比在相同体积的密闭容器中加入起始物质,平衡时SO3的物质的量大于W mol的是
A.2molSO2 、1molO2 B.4molSO2 、1molO2
C.2molSO2 、1molO2 、2mol SO3 D.1molSO2 、2mol SO3
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市十三校高三第二次联考化学试卷(解析版) 题型:选择题
将0.5 mol·L-1的Na2CO3溶液与amol·L-1的NaHCO3溶液等体积混合,所得溶液中粒子浓度间的关系及相关判断正确的是
A.c(Na+)>2c(CO32-)+c(HCO3-)+c(OH-)
B.c(Na+)>c(CO32-)+c(HCO3-)+c(H2CO3)
C.若c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+),则可确定a>0.5
D.若c(CO32-)+2c(OH-) = 2c(H+)+c(HCO3-)+3c (H2CO3), 则可确定a=0.5
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:简答题
(14分)脱去冶金工业排放烟气中SO2的方法有多种。
(1)热解气还原法。已知CO还原SO2生成S(g)和CO2过程中, 每转移1mol电子需吸收2.0 kJ的热量,则该反应的热化学方程式为 。
每转移1mol电子需吸收2.0 kJ的热量,则该反应的热化学方程式为 。
(2)离子膜电解法。利用硫酸钠溶液吸收SO2,再用惰性电极电解。将阴极区溶液导出,经过滤分离硫磺后,可循环吸收利用,装置如图1所示,则阴极的电极反应式为 ,阳极产生气体的化学式为 。

(3)氧化锌吸收法。配制ZnO悬浊液(含少量MgO、CaO) ,在吸收塔中封闭循环脱硫,发生的主要反应为ZnO+SO2 = ZnSO3(s),测得pH、吸收效率η随时间t的变化如图2所示。
,在吸收塔中封闭循环脱硫,发生的主要反应为ZnO+SO2 = ZnSO3(s),测得pH、吸收效率η随时间t的变化如图2所示。
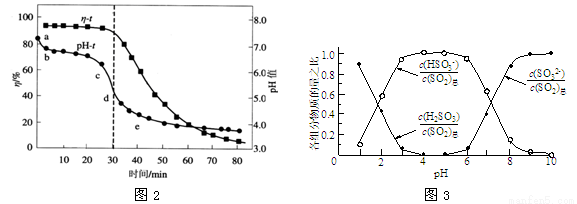
①该反应常温能自发进行的原因是 。
②纯ZnO的悬浮液pH约为6.8,结合图2和图3,下列说法正确的是 。
A.向ZnSO3与水混合体系中加稀硫酸,硫元素会以SO2形式逸出
B.pH-t曲线ab段发生的主要反应为ZnO+SO2=ZnSO3
C.pH-t曲线cd段发生的主要反应为ZnSO3+SO2+H2O = Zn (HSO3)2
D.pH=7时,溶液中c(SO32-) = c(HSO3-)
③为提高SO2的吸收效率η,可采取的措施为 。
A.增大悬浊液中ZnO的量
B.适当提高单位时间内烟气的循环次数
C.调节溶液的pH 至6.0以下
至6.0以下
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com