
【题目】铝用途广泛,用铝土矿(主要成分为Al2O3nH2O、少量SiO2和Fe2O3)制取Al有如下途径: 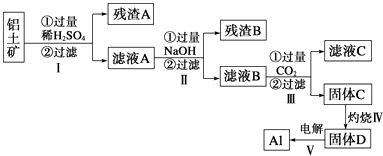
(1)滤液A加过量NaOH离子方程式表示为
(2)灼烧时盛放药品的仪器名称是 .
(3)步骤Ⅳ中发生反应的化学方程式是 .
(4)步骤Ⅲ中生成固体C的离子反应方程式为 .
(5)取滤液B 100mL,加入1molL﹣1盐酸200mL,沉淀量达到最大且质量为11.7g.则滤液B中c(AlO ![]() )= , c(Na+)6molL﹣1(填“>”、“=”或“<”).
)= , c(Na+)6molL﹣1(填“>”、“=”或“<”).
【答案】
(1)4OH﹣+Al3+═AlO2﹣+2H2O、Fe3++3OH﹣═Fe(OH)3↓
(2)坩埚
(3)2Al(OH)3 ![]() Al2O3+3H2O
Al2O3+3H2O
(4)AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣
(5)1.5mol?L﹣1;>
【解析】解:(1)根据以上分析,滤液A中含有Al2(SO4)3、Fe(SO4)3 , 加入过量NaOH故反应的离子方程式为4OH﹣+Al3+═AlO2﹣+2H2O、Fe3++3OH﹣═Fe(OH)3↓; 故答案:4OH﹣+Al3+═AlO2﹣+2H2O、Fe3++3OH﹣═Fe(OH)3↓;(2)根据加热溶液一般在蒸发皿里进行,而固体一般在坩埚中进行,故答案:坩埚;(3)根据以上分析,固体C为氢氧化铝,所以步骤Ⅳ中发生反应的化学方程式2Al(OH)3 ![]() Al2O3+3H2O;故答案:2Al(OH)3
Al2O3+3H2O;故答案:2Al(OH)3 ![]() Al2O3+3H2O;(4)步骤Ⅲ中生成固体C的反应是向滤液B中通入二氧化碳气体,又根据以上分析,滤液B中含有NaAlO2 , 故反应的离子方程式:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣;故答案:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣;(5)根据以上分析滤液B中含有硫酸钠、偏铝酸钠、过量的氢氧化钠,向滤液中加入1mol/L盐酸200mL,沉淀量达到最大且质量为11.7g为Al(OH)3的质量,则根据铝原子守恒,c(AlO
Al2O3+3H2O;(4)步骤Ⅲ中生成固体C的反应是向滤液B中通入二氧化碳气体,又根据以上分析,滤液B中含有NaAlO2 , 故反应的离子方程式:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣;故答案:AlO2﹣+CO2+2H2O═Al(OH)3↓+HCO3﹣;(5)根据以上分析滤液B中含有硫酸钠、偏铝酸钠、过量的氢氧化钠,向滤液中加入1mol/L盐酸200mL,沉淀量达到最大且质量为11.7g为Al(OH)3的质量,则根据铝原子守恒,c(AlO ![]() )=
)= ![]() =
= ![]() =1.5molL﹣1
=1.5molL﹣1
最后所得的溶液中溶质为硫酸钠、氯化钠,根据钠离子守恒有n(NaOH)=n(NaCl)+2(Na2SO4),根据氯离子与硫酸根守恒有n(NaCl)=n(HCl)=0.2L×1mol/L=0.2mol,n(Na2SO4)=n(H2SO4)>3n(Al2(SO4)3)=3× ![]() mol=0.45mol,故n(NaOH)=n(NaCl)+2(Na2SO4)>0.2mol+2×0.45mol=1.1mol,故c(Na+)>
mol=0.45mol,故n(NaOH)=n(NaCl)+2(Na2SO4)>0.2mol+2×0.45mol=1.1mol,故c(Na+)> ![]() =11mol/L,
=11mol/L,
故答案:1.5molL﹣1;>;


科目:高中化学 来源: 题型:
【题目】硫酸铁(PFS)是一种新型高效的无机高分子絮凝剂,广泛用于水的处理。用铁的氧化物为原料来制取聚合硫酸铁,为控制水解时Fe3+的浓度,防止生成氢氧化铁沉淀,原料中的Fe3+必须先还原为Fe2+。实验步骤如下:
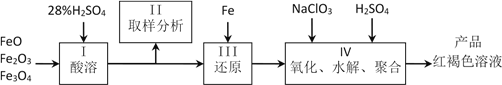
(1)用98%的硫酸配制28%的硫酸,所需的玻璃仪器除量筒外,还有____________。
(a) 容量瓶 (b) 烧杯 (c) 烧瓶
(2)步骤II取样分析溶液中的Fe2+、Fe3+的含量,目的是____________。
(a) 控制溶液中Fe2+与Fe3+含量比 (b) 确定下一步还原所需铁的量
(c) 确定氧化Fe2+所需NaClO3的量 (d) 确保铁的氧化物酸溶完全
(3)用NaClO3氧化时反应方程式如下:6FeSO4 + NaClO3 + 3H2SO4 → 3Fe2(SO4)3 + NaCl + 3H2O
若改用HNO3氧化,则反应方程式如下6FeSO4 + 2HNO3 + 3H2SO4 → 3Fe2(SO4)3 + NO↑ + 4H2O
已知1mol HNO3价格0.16元、1mol NaClO3价格0.45元,评价用HNO3代替NaClO3作氧化剂的得弊,利是____________________,弊是________________________。聚合硫酸铁溶液中SO42与Fe3+物质的量之比不是3:2。根据下列供选择的试剂和基本操作,测定聚合硫酸铁产品溶液中SO42与Fe3+物质的量之比。
(4)测定时所需的试剂____________。
(a) NaOH (b) FeSO4 (c) BaCl2 (d) NaClO3
(5)需要测定____________和____________的质量(填写化合物的化学式)。
(6)选出测定过程中所需的基本操作____________(按操作先后顺序列出)。
(a) 萃取、分液 (b) 过滤、洗涤 (c) 蒸发、结晶
(d) 冷却、称量 (e)烘干或灼烧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,10 mL 0.40 mol/L H2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表。
t/min | 0 | 2 | 4 | 6 | 8 | 10 |
V(O2)/mL | 0.0 | 9.9 | 17.2 | 22.4 | 26.5 | 29.9 |
下列叙述不正确的是(溶液体积变化忽略不计)( )
A. 0~6 min的平均反应速率: v(H2O2)≈3.3×10-2mol·L-1·min-1
B. 0~6 min的平均反应速率: v(H2O2)<3.3×10-2mol·L-1·min-1
C. 反应至6 min时,c(H2O2)=0.30 mol/L
D. 反应至6 min时,H2O2分解了50%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某无色透明的碱性溶液中,能大量共存的离子组是( )
A. Na+、Ca2+、HCO3-、NO3-
B. AlO2-、K+、CO3 2-、Na+
C. Al3+、Cl-、CO32-、Na+
D. MnO4-、K+、Na+、NO3 -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝用途广泛,用铝土矿(主要成分为Al2O3nH2O、少量SiO2和Fe2O3)制取Al有如下途径: 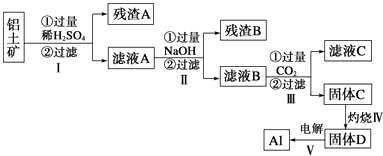
(1)滤液A加过量NaOH离子方程式表示为
(2)灼烧时盛放药品的仪器名称是 .
(3)步骤Ⅳ中发生反应的化学方程式是 .
(4)步骤Ⅲ中生成固体C的离子反应方程式为 .
(5)取滤液B 100mL,加入1molL﹣1盐酸200mL,沉淀量达到最大且质量为11.7g.则滤液B中c(AlO ![]() )= , c(Na+)6molL﹣1(填“>”、“=”或“<”).
)= , c(Na+)6molL﹣1(填“>”、“=”或“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在实验室里可用如图所示装置来制取氯酸钠、次氯酸钠和探究氯水的性质. 图中:
①为氯气发生装置;
②的试管里盛有15mL30%NaOH溶液来制取氯酸钠,并置于热水浴中;
③的试管里盛有15mL8%NaOH溶液来制取次氯酸钠,并置于冰水浴中;
④的试管里加有紫色石蕊试液;
⑤为尾气吸收装置.
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过(仪器名称)向烧瓶中加入适量的浓盐酸.实验室制Cl2的化学方程式为; 实验时为了除去氯气中的HCl气体,可在①与②之间安装盛有(填写下列编号字母)的净化装置.
A.碱石灰 B.氢氧化钠溶液 C.饱和食盐水 D.浓硫酸
(2)如果将过量二氧化锰与20mL12molL﹣1的浓盐酸混合加热,充分反应后生成的氯气0.06mol.(填“大于”“小于”或“等于”),若有17.4g的MnO2被还原,则被氧化的HCl的物质的量为 .
(3)写出装置②中发生反应的化学方程式 .
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白.
实验现象 | 原因 |
溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
随后溶液逐渐变为无色 | |
然后溶液从无色逐渐变为色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于1.0molL﹣1 Na2SO4溶液的叙述正确的是( ) ①溶液中含有1mol Na2SO4②1L溶液中含有142g Na2SO4
③将1mol Na2SO4溶于1mol水中所得的溶液④将322g Na2SO410H2O溶于水后再稀释成1 000mL所得的溶液.
A.①③
B.②④
C.③④
D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,某溶液中由水电离的 c(H+)=1×10-13mol·L-1,该溶液可能是 ( )
①SO2 水溶液 ② NH4Cl 溶液 ③ NaNO3 溶液 ④ NaOH 溶液
A. ①④ B. ①② C. ②③ D. ③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有①乙酸乙酯和碳酸钠溶液②甲醇和乙醇③溴化钠和溴水三组混合物,分离它们的正确方法依次是( )
A. 分液 蒸馏 萃取 B. 蒸馏 萃取 分液
C. 分液 萃取 蒸馏 D. 萃取 蒸馏 分液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com