
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:解答题
 A、B、C、D、E五种元素,其元素性质或原子结构相关信息如表:
A、B、C、D、E五种元素,其元素性质或原子结构相关信息如表:| 元素编号 | 元素性质或原子结构 |
| A | M层全满,N层没有成对电子 |
| B | 第3周期第13列元素 |
| C | 元素的最高价氧化物与它的气态氢化物反应得到离子化合物 |
| D | 基态原子有9种不同的运动状态 |
| E | 基态原子共有4个能级,没有未成对电子 |
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 不慎把浓硫酸沾在手上,立即用水冲洗,再涂上小苏打溶液 | |
| B. | 如果汽油、煤油等可燃物着火,应立即用水扑灭 | |
| C. | 不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上稀盐酸溶液 | |
| D. | 酒精灯不慎碰翻着火,应立即用湿布盖灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 通过计算得出:应量取12mol/L的浓盐酸8.0mL | |
| B. | 向容量瓶中加水定容时俯视标线,所配溶液浓度偏高 | |
| C. | 用量筒量取所需的浓盐酸时俯视刻度线,所配溶液浓度偏高 | |
| D. | 定容摇匀后发现液面最低点低于标线,再补几滴水所配溶液浓度偏高 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
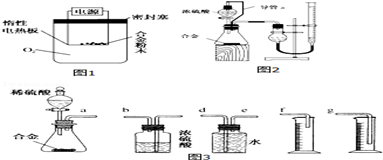
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与28 g CO具有相同分子数的CO2的质量一定是44 g | |
| B. | 与V L CO具有相同分子数的CO2的体积一定是V L | |
| C. | 等质量的H2S和PH3含有相同的原子数 | |
| D. | 同温同压下,相同体积的物质,其物质的量一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| B. | SO2+H2O+Ca2++2ClO-═CaSO4↓+HClO+H++Cl- | |
| C. | 2SO2+2H2O+Ca2++2ClO-═CaSO4↓+4H++2Cl-+SO${\;}_{4}^{2-}$ | |
| D. | SO2+H2O+Ca2++3ClO-═CaSO4↓+2HClO+Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com