
分析 (1)有机分子中碳原子连四个不同的原子或原子团时,称为不对称碳原子(或手性碳原子),以*C表示,具有手性碳原子的有机物具有光学活性;
(2)①Cr位于周期表第四周期ⅥB族,原子核外电子排布为1s22s22p63s23p63d54s1,失去3个电子生成Cr3+,配合物[Cr(H2O)6]3+中Cr3+为中心离子,H2O为配体;
②CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子,CH3CHOOH分子中含有1个C-C、3个C-H、1个C-O、1个C=O、1个O-H等化学键;
③与H2O互为等电子体的阳离子应含有3个原子、且电子数为10,H2O与CH3CH3OH都含有氢键,且都为极性分子,二者互溶.
解答 解:(1)CH2OH-CHOH-CH2OH分子中不存在手性碳原子,没有光学活性;CH3-CHOH-COOH中间碳是手性碳原子;CH2OH-CHOH-CHOH-CH2-CHO从到起第二个碳和第三个碳是手性碳原子,故答案为:B;C;
(2)①Cr位于周期表第四周期ⅥB族,原子核外电子排布为1s22s22p63s23p63d54s1,失去3个电子生成Cr3+,则离子的电子排布为1s22s22p63s23p63d3,
配合物[Cr(H2O)6]3+中Cr3+为中心离子,H2O为配体,O原子提供孤对电子,与Cr3+形成配位键,
故答案为:1s22s22p63s23p63d3;O;
②CH3COOH中C原子分别形成4个、3个δ键,没有孤对电子,分别为sp3杂化、sp2杂化,CH3CHOOH分子中含有1个C-C、3个C-H、1个C-O、1个C=O、1个O-H等化学键,则1mol CH3COOH分子中含有σ键的数目为7mol或7×6.02×1023,
故答案为:sp3和sp2;7mol或7×6.02×1023;
③与H2O互为等电子体的阳离子应含有3个原子、且电子数为10,应为H2F+,H2O与CH3CH2OH都含有氢键,且都为极性分子,二者互溶,
故答案为:H2F+;H2O与乙醇分子间形成氢键.
点评 本题综合考查原子结构与元素的性质,题目涉及核外电子排布、杂化类型以及等电子体等问题,侧重于学生的分析能力的考查,注意把握相关知识的判断方法,难度不大.


科目:高中化学 来源: 题型:选择题
| A. | NH4+、NO3-、Al3+、K+ | B. | Na+、NO3-、S2-、K+ | ||
| C. | MnO4-、SO32-、Na+、K+ | D. | HCO3-、SO42-、Na+、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HCl MgCl2 NH4Cl | B. | H2O Na2O2 ? CO2 | ||
| C. | CaCl2 NaOH H2O | D. | CH4 H2O CS2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 外界条件可以改变平衡状态 | B. | 达到平衡时正、逆反应速率相等 | ||
| C. | 平衡时各组分的含量也在不断变化 | D. | 该反应所建立的平衡是动态平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,22.4L二氯甲烷的分子数约为NA个 | |
| B. | 1mol冰中有2mol氢键 | |
| C. | 17.6g丙烷中所含的极性共价键为3.2NA个 | |
| D. | 1molH3O+含有11mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
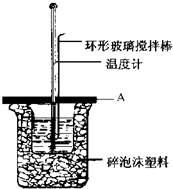 实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1NaOH溶液利用上图装置,进行测定中和热的实验.假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g•℃).为了计算中和热,实验时还需测量的数据有(填序号)ACE.
实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1NaOH溶液利用上图装置,进行测定中和热的实验.假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g•℃).为了计算中和热,实验时还需测量的数据有(填序号)ACE.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
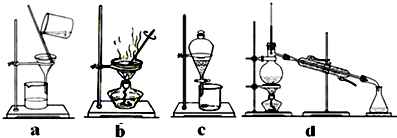
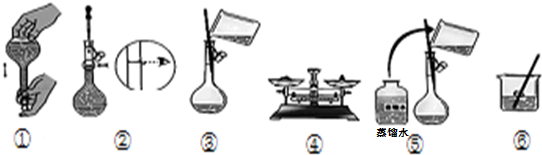
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 乳酸[CH3CH(OH)COOH]中存在一个手性碳原子 | |
| C. | 许多过渡金属离子对多种配体具有很强的结合力,因而,只有过渡金属才能形成配合物 | |
| D. | 已知酸性:H3PO4>HClO,是因为H3PO4分子中有1个非羟基氧原子而HClO为0 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Y可能为气态 | B. | Y一定为固态或液态 | ||
| C. | Z可能为气态 | D. | Z一定为固态或液态 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com