
| 电离能 /(kJ•mol-1) | I1 | I2 | I3 | I4 |
| A | 932 | 1821 | 15390 | 21771 |
| B | 738 | 1451 | 7733 | 10540 |
分析 (1)同周期随原子序数增大,电负性增大,同主族自上而下电负性减小;根据晶体的类型与熔沸点的关系解答,原子晶体的溶沸点大于分子晶体;
(2)由表中数据可知A、B最外层电子数为2,位于相同主族,根据电离能的大小可知B为Mg元素,根据能量最低原理书写电子排布式;
(3)判断Mn2+离子的原子核外3d轨道上是否含有电子来判断是否有颜色;
(4)①C=O键中含有1个δ键,1个π键;②配合物中提供孤电子对的分子或离子为配位体.
解答 解:(1)同周期随原子序数增大,电负性增大,同主族自上而下电负性减小,故电负性:N>C>Si,C60是分子晶体,熔化需破坏分子间作用力,而金刚石是原子晶体,原子晶体的熔化需破坏共价键,所以其熔沸点远大于分子晶体,
故答案为:N>C>Si;金刚石;
(2)由表中数据可知A、B最外层电子数为2,位于相同主族,根据电离能的大小可知B为Mg元素,原子序数为12,核外电子排布式为1s22s22p63s2,
故答案为:1s22s22p63s2;
(3)Mn2+离子的原子核外排布式为1s22s22p63s23p63d5,其d轨道上有5的电子,故[Mn(H2O)6]2+ 有颜色,
故答案为:有;
(4)①C=O键中含有1个δ键,1个π键,则COCl2分子内含有3个σ键、1个π键,所以C原子为sp2杂化,
故答案为:3;1;sp2;
②配合物Fe(CO)5中CO提供孤电子对,所以其配体是CO,故答案为:CO.
点评 本题考查较为综合,涉及电负性、晶体类型、化学键等多个方面的知识,注意晶体类型以及对数据的分析和判断,学习中注重相关基础知识和解题方法的积累,题目中等难度.


科目:高中化学 来源: 题型:选择题
| A. | (1) | B. | (2) | C. | (3) | D. | (4) |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2溶液与酸性KMnO4溶液反应:2MnO4-+3H2O2+6H+═2Mn2++6H2O+4O2↑ | |
| B. | 向Fe(NO3)3溶液中加入过量的HI溶液:2 NO3-+8H++6I-═3I2+2NO↑+4H2O | |
| C. | 少量SO2通入碳酸钠溶液中:CO32-+SO2═CO2+S O32- | |
| D. | 0.01 mol•L-1 NH4Al(SO4)2溶液与0.02 mol•L-1 Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+Al(OH)3↓+NH3•H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 酚类化合物有毒,不能用于杀菌消毒 | |
| B. | 乙烯可催熟水果 | |
| C. | 石油的裂解可获得乙烯、丙烯等短链烯烃 | |
| D. | 甲醛的水溶液可用于防腐 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
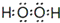 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | r(Na+)>r(Na) | B. | r(Cl-)>r(Cl) | C. | r(Ca2+)>r(Cl-) | D. | r(Mg)>r(Na) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com