
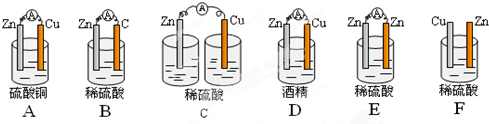
分析 构成原电池需具备以下条件:两个活性不同的电极;电解质溶液;形成闭合回路;存在能自动发生的氧化还原反应,且为放热反应,以此来解答.
解答 解:原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应.原电池中正极上发生还原反应,负极上发生氧化反应,据此可知装置AB能构成原电池,电池总反应方程式分别为:CuSO4+Zn═ZnSO4+Cu;H2SO4+Zn═ZnSO4+H2↑,
答:AB装置可以构成原电池;A中电池总反应CuSO4+Zn═ZnSO4+Cu;B中电池总反应H2SO4+Zn═ZnSO4+H2↑;
(2)C、F没有形成闭合回路,不能构成原电池;D中酒精是非电解质,不能构成原电池;E中电极相同,不能构成原电池,
答:C、F没有形成闭合回路,不能构成原电池;D中酒精是非电解质,不能构成原电池;E中电极相同,不能构成原电池.
点评 本题考查了原电池原理的分析应用,该题是高考中的常见考点,属于基础性试题的考查,难度不大.明确原电池的工作原理、构成条件是答题的关键.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | R一定是第2周期元素 | |
| B. | R一定是VA族元素 | |
| C. | R的气态氢化物一定比同周期其他元素气态氢化物稳定 | |
| D. | R气态氢化物化学式为H2R |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | 只有②④ | C. | 只有①②③ | D. | 只有④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
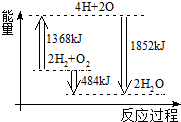
| A. | 拆开2 mol H2(g)和1 mol O2(g)中的化学键成为H、O原子,共放出1368 kJ能量 | |
| B. | 由H、O原子形成2 mol H2O(g),共吸收1852 kJ能量 | |
| C. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),共吸收484 kJ能量 | |
| D. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com