
| A. | 44g CO2 | B. | 11.2L H2 | C. | 2mol Fe | D. | 2mol H2O |
 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:高中化学 来源: 题型:选择题
| A. | 由石油制取乙烯、丙烯等化工原料不涉及化学变化 | |
| B. | “神州七号”的防护层中含聚四氟乙烯,制备聚四氟乙烯的单体属于不饱和烃 | |
| C. | 浓硫酸可用于干燥SO2、C2H4、O2等气体 | |
| D. | 用CO2合成可降解的聚碳酸酯塑料,可以实现“碳”的循环利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
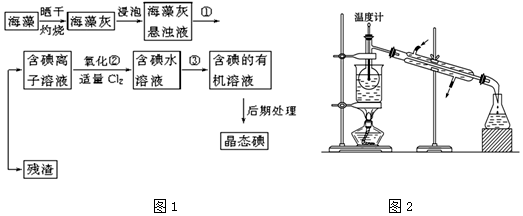
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
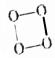 的O4是一种价格超过黄金的气体,下列有关O4的说法中不正确的是( )
的O4是一种价格超过黄金的气体,下列有关O4的说法中不正确的是( )| A. | O4与O3、O2互为同素异形体 | |
| B. | O4与H2反应生成冰 | |
| C. | O4中各原子最外电子层均达到8电子结构 | |
| D. | O4的化学性质一定比O2稳定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2LC2H5OH含有的氢原子数为3NA | |
| B. | 25℃时,1LpH=12的碳酸钠溶液中含有Na+的数目为0.02NA | |
| C. | 过氧化钠与水反应时,生成0.5molO2转移的电子数为NA | |
| D. | 2molSO2和1molO2在一定条件下充分反应,所得混合气体的分子数等于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 固体活性炭/mol | NO/mol | A/mol | B/mol | |
| 200℃ | 2.000 | 0.0400 | 0.0300 | 0.0300 |
| 335℃ | 2.005 | 0.0500 | 0.0250 | 0.0250 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2 mol的铁与足量的稀硝酸反应,生成气体的分子数目为0.3 NA | |
| B. | 常温常压下,14 g由 C2H4、C3H6组成的混合气体中含有碳原子的数目为NA | |
| C. | 2.24 L CO2与足量的Na2O2反应,转移的电子总数必为0.1NA | |
| D. | l Ll mol/L的KAl(SO4)2溶液中阳离子总数为2 NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com