
����Ŀ��Ϊ��֤�����ԣ�Cl2��Fe3+��SO2��ij��ѧ�о���ѧϰС������ͼ��ʾװ�ý���ʵ�飨�г�������A�еļ���װ�����ԣ��������Ѿ�������ϣ���
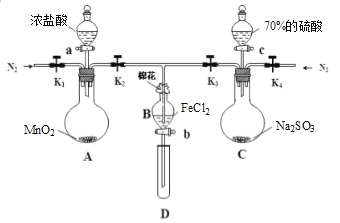
�������ɼ�K1��K4��ͨ��һ��ʱ��N2���ٽ�T�͵��ܲ���B�У�����ͨ��N2��Ȼ��ر�K1��K3��K4��
��������a���μ�һ������Ũ���ᣬ��A������
������B����Һ���ʱ��ֹͣ���ȣ��н����ɼ�K2��
��������b��ʹԼ2mL����Һ����D�Թ��У��������е���������
�������ɼ�K3������c������70%�����ᣬһ��ʱ���н����ɼ�K3��
���������Թ�D���ظ�������������B��Һ�е�������
��1����������Ŀ����__________________________________________________________��
��2�����н������ҺΪ________________��������_____________________________________________ ��
��3��A�з�����Ӧ�Ļ�ѧ����ʽ________________________________________________��
��4�����²���������Һ��Ƶ����ӷ�Ӧ��________________________________________����________��д�Լ���ѧʽ�������������������____________________________________________ ��
��5����˵��������Fe3+��SO2�����ӷ���ʽ��_______________________________��
��6���ס��ҡ�����λͬѧ�ֱ����������ʵ�飬���ǵļ����һ���ܹ�֤��������:Cl2��Fe3+��SO2����_______��������������������������
��������B��Һ�к��е����� | ��������B��Һ�к��е����� | |
�� | ��Fe3+��Fe2+ | ��SO42�� |
�� | ����Fe3+����Fe2+ | ��SO42�� |
�� | ��Fe3+��Fe2+ | ��Fe2+ |
���𰸡� ����װ���ڵĿ��� aOH��Һ �����ݳ���Cl2��SO2 MnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O 2Fe2++Cl2=2Fe3++2Cl- KSCN��Һ ��Һ��ΪѪ��ɫ 2Fe3++SO2+2H2O=2Fe2++4H++SO42- �Һͱ�
MnCl2+Cl2��+2H2O 2Fe2++Cl2=2Fe3++2Cl- KSCN��Һ ��Һ��ΪѪ��ɫ 2Fe3++SO2+2H2O=2Fe2++4H++SO42- �Һͱ�
����������1�����ɼ�K1��K4��ͨ��һ��ʱ��N2��Ŀ�����ų�װ���е���������ȷ�𰸣�����װ���ڵĿ��� ��
(2) ���н����Ϊ����������Һ�����ܹ����շ�Ӧ�ж���������������������壬��ֹ��Ⱦ��������ȷ�𰸣�NaOH��Һ �������ݳ���Cl2��SO2 ��
��3��A��Ϊ����������Ũ������ȷ�Ӧ�����������Ȼ��̺�ˮ����Ӧ�Ļ�ѧ����ʽ��MnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O����ȷ����MnO2+4HCl(Ũ)
MnCl2+Cl2��+2H2O����ȷ����MnO2+4HCl(Ũ) ![]() MnCl2+Cl2��+2H2O��
MnCl2+Cl2��+2H2O��
��4����������ǿ���������ܹ����Ȼ���������Ϊ�Ȼ�����������������Һ�Ի�ɫ�����ӷ�Ӧ�ǣ�2Fe2++Cl2=2Fe3++2Cl-�����������к��������������������軯����Һ���м����������Һ��ΪѪ��ɫ��֤������������������ȷ����2Fe2++Cl2=2Fe3++2Cl- ��KSCN��Һ����Һ��ΪѪ��ɫ��
��5��Fe3+�����������°Ѷ�����������Ϊ�����������������ԭΪFe2+������˵��������Fe3+��SO2�����ӷ���ʽΪ��2Fe3++SO2+2H2O=2Fe2++4H++SO42-����ȷ����2Fe3++SO2+2H2O=2Fe2++4H++SO42-��
��6�����е�һ����Fe3+��Fe2+�������������Դ��������ӣ����еڶ��κ���SO42���������ǹ����������Ѷ�����������ΪSO42������һ����Fe3+�Ѷ������������������״���
���е�һ�μ���Fe3+����Fe2+��˵���������㣬���������Դ��������ӣ����еڶ��κ���SO42����˵�������˶��������������ӵķ�Ӧ�������������Ӵ��ڶ�����������˿���֤��������:Cl2��Fe3+��SO2������ȷ��
���е�һ����Fe3+��Fe2+�������������Դ��������ӣ��ڶ�����Fe2+��˵�����������������������ӵķ�Ӧ���������������Ӵ��ڶ�����������˿���֤��������:Cl2��Fe3+��SO2������ȷ��������������ȷѡ���ҡ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��X��Y��Z��L��M����Ԫ�ص�ԭ��������������X��Y��Z��L����ɵ����ʵĻ���Ԫ�أ�M�ǵؿ��к�����ߵĽ���Ԫ�أ�
�ش��������⣺
��1��L��Ԫ�ط���Ϊ��M��Ԫ�����ڱ��е�λ��Ϊ������Ԫ�ص�ԭ�Ӱ뾶�Ӵ�С��˳��������Ԫ�ط��ű�ʾ����
��2��Z��X��Ԫ�ذ�ԭ����Ŀ��l��3��2��4���ɷ���A��B��A�ĵ���ʽΪ �� B�ĽṹʽΪ ��
��3������se��������������Ԫ�أ���Lͬһ���壬Seԭ�ӱ�Lԭ�Ӷ��������Ӳ㣬��Se��ԭ������Ϊ �� ������������Ӧ��ˮ���ﻯѧʽΪ �� ����2��5����Ԫ�ص��ʷֱ���H2��Ӧ����l mol��̬�⻯��ķ�Ӧ�����£���ʾ����1mol�����ⷴӦ�ȵ���������ĸ���ţ���
a��+99.7molL��1 b��+29.7molL��1 c����20.6molL��1 d����241.8kJmol��1 ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��0.5 mol��Fe��_______����ԭ�ӣ���6.02��1023��ʾ�����ӵ���������������_____g��
��2��3mol CO2�ڱ�״���µ����Ϊ___________L��Ħ������Ϊ______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������������IJ�����ߣ��ϵ�ر�����м��д��������ⱻ�ᵽ�����ճ̣�����Ҫԭ���ǣ�������
A.���õ����ǵĽ�������
B.��ֹ����й����Ӻ�Ǧ���ؽ������Ӷ�������ˮԴ�����Ⱦ
C.��ʹ��������ĵ��Һ��ʴ������Ʒ
D.��������ʯī�缫
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л���� 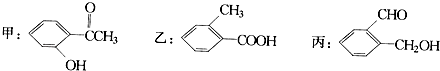
��1����д�����к��������ŵ����ƣ� ��
��2�����б�������Щ�����ﻥΪͬ���칹�壺 ��
��3����ֱ�д������ס��ҡ���������ķ�������ָ����ѡ�Լ�����Ҫ���ɣ�
����ķ�������
�����ҵķ�������
������ķ����� ��
��4���밴������ǿ�������мס��ҡ�����˳�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ײ��ϡ�������ֱ��Ϊ1��100 nm��1nm=10-9m)�IJ��ϣ�����̼��������һ�֣���������̼���ȵط�ɢ������ˮ�У����γɵ����� ������Һ�����ǽ��塡���ܲ��������ЧӦ����������ֽ���ݲ�������ֽ�����ú��������ɫ��������ȷ��ѡ���У�
A.�٢ܢ�B.�ڢۢ�C.�ڢۢ�D.�٢ۢܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��2016��8��5���ڰ�����Լ�ٿ��ĵ�31����˻ᣬ�����˷ܼ��¼���ʹ��������˹�˶�Ա���������ֹ�˶�Աʹ���˷ܼ��ǰ��˻ṫƽ����������Ҫ�ٴ�֮һ�������������˷ܼ��Ľṹ�ֱ�Ϊ�� 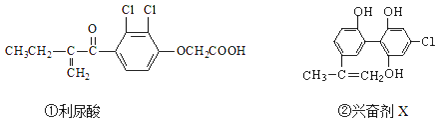
��������������˷ܼ���˵���в���ȷ���ǣ�������
A.�������ܷ���ȡ����Ӧ���ӳɷ�Ӧ��������Ӧ
B.1mol�˷ܼ�X������Ũ��ˮ��Ӧ���������3molBr2
C.����FeCl3��Һ������������Ƿ����˷ܼ�X
D.1mol�˷ܼ�X���ܺ�5molNaOH����Һ��Ӧ
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com