
【题目】肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料。实验室可用苯甲醛和乙酸酐、醋酸钠等原料经下列反应制取肉桂酸,其中苯甲醛为无色油状液体。已知:
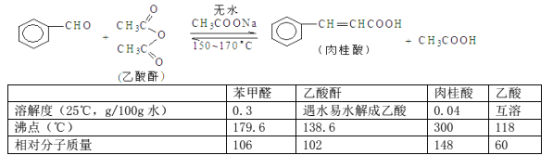
填空:
Ⅰ.合成:反应装置如图所示。向三颈烧瓶中先后加入研细的无水醋酸钠、4.8g苯甲醛和5.6g乙酸酐,振荡使之混合均匀。在150~170℃加热1小时,保持微沸状态。
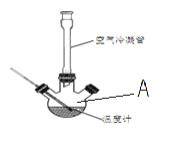
(1)仪器A的名称为___。
(2)空气冷凝管的作用是__,该装置加热要控制反应呈微沸状态,如果剧烈沸腾,会导致肉桂酸产率降低,可能的原因是__。
(3)不能把无水CH3COONa换成CH3COONa·3H2O的原因是__。
Ⅱ.粗品精制:已知水蒸气蒸馏是分离提纯有机化合物的重要方法之一,可使待提纯的有机物在低于100℃的情况下随水蒸气一起被蒸馏出来,从而达到分离提纯的目的。
将上述反应后得到的混合物趁热倒入圆底烧瓶中,进行下列操作:
a.在搅拌下,向反应液中加入20mL水
b.再慢慢加入碳酸钠溶液
c.然后进行水蒸气蒸馏
d.待烧瓶内溶液冷却至室温,在搅拌下用加入盐酸酸化,析出大量晶体,过滤,洗涤,干燥。
(4)饱和Na2CO3溶液的作用有__。水蒸气蒸馏可除去的杂质是__;如何判断蒸馏终点___。
(5)若得到的肉桂酸晶体产品不纯,应采用__可得到纯度更高的产品。
(6)若最后得到纯净的肉桂酸5.0g,则该反应中的产率是__(保留两位有效数字)。
【答案】三颈烧瓶 使反应物冷凝回流 乙酸酐蒸出,反应物减少,平衡逆向移动 CH3COONa·3H2O受热生成水会使乙酸酐水解 将肉桂酸转化为肉桂酸钠,溶于水,中和乙酸 苯甲醛 当当流出液澄清透明不再含有有机物质的油滴时,即可断定水蒸汽蒸馏结束(其他答案合理也行) 重结晶 75%
【解析】
⑴根据图得出该仪器的名称。
⑵根据表格各物质的沸点可知,反应物在这个条件下易挥发,所以空气冷凝管作用是使反应物冷凝回流,该反应在150~170℃的条件下进行,在150~170℃时乙酸酐易挥发,如果剧烈沸腾,乙酸酐蒸出,反应物减少。
⑶根据信息乙酸酐遇水易水解成乙酸,而CH3COONa·3H2O受热生成水。
⑷饱和Na2CO3溶液的作用除去生成的乙酸,并将肉桂酸转化为肉桂酸钠;水蒸气蒸馏可除去苯甲醛,当流出液澄清透明不再含有有机物质的油滴时,即可断定水蒸汽蒸馏结束。
⑸提高纯度可以用重结晶。
⑹先计算理论上得到肉桂酸的质量,再计算产率。
⑴该仪器的名称为三颈烧瓶;故答案为:三颈烧瓶。
⑵该反应在150~170℃的条件下进行,根据表格各物质的沸点可知,反应物在这个条件下易挥发,所以空气冷凝管作用是使反应物冷凝回流,使反应物充分反应,该反应在150~170℃的条件下进行,在150~170℃时乙酸酐易挥发,如果剧烈沸腾,乙酸酐蒸出,反应物减少,平衡逆向移动;故答案为:使反应物冷凝回流;乙酸酐蒸出,反应物减少,平衡逆向移动。
⑶根据信息乙酸酐遇水易水解成乙酸,而CH3COONa·3H2O受热生成水,水会使乙酸酐水解生成乙酸;故答案为:CH3COONa·3H2O受热生成水会使乙酸酐水解。
⑷饱和Na2CO3溶液的作用除去未反应的原料乙酸酐,中和生成的乙酸,并将肉桂酸转化为肉桂酸钠,增大它在水中的溶解性;水蒸气蒸馏可除去苯甲醛,当流出液澄清透明不再含有有机物质的油滴时,即可断定水蒸汽蒸馏结束(也可用盛有清水的锥形瓶或烧杯来检查是否有油珠存在);故答案为:将肉桂酸转化为肉桂酸钠,溶于水,中和乙酸;苯甲醛;当流出液澄清透明不再含有有机物质的油滴时,即可断定水蒸汽蒸馏结束(其他答案合理也行)。
⑸提高纯度可以用重结晶;故答案为:重结晶。
⑹4.8g苯甲醛理论上得到肉桂酸的质量为![]() ,则产率为
,则产率为![]() ;故答案为:75%。
;故答案为:75%。


科目:高中化学 来源: 题型:
【题目】“碘伏”又叫“聚维酮碘溶液”。聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图所示。下列说法正确的是
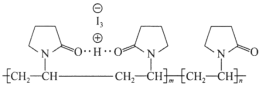 (图中虚线表示氢键)
(图中虚线表示氢键)
A.C、N、O原子的电负性依次增大
B.聚维酮碘中含有离子键、共价键、氢键等化学键
C.聚维酮易溶于水的原因是与水分子间形成氢键
D.分子中的含N五元环一定是平面结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列说法正确的是( )
A.0.1molH2和0.1molI2(g)于密闭容器中充分反应,容器内原子总数为0.2NA
B.常温常压下,28gFe和足量浓硝酸混合,转移电子数为1.5NA
C.标准状况下22.4LHF中含有的氟原子数目为NA
D.2gD2O和H2l8O混合物中所含中子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在硫酸铝、硫酸钾和明矾的混合溶液中,硫酸根离子的浓度为0.4mol·L-1,当加入等体积0.4mol·L-1氢氧化钾溶液时,生成的沉淀恰好完全溶解。则反应后溶液中钾离子的浓度约为( )
A.0.225mol·L-1B.0.25mol·L-1C.0.45mol·L-1D.0.9mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中和滴定不仅可以测定酸或碱的物质的量浓度,还可以测定某些混合物的含量。
烧碱是重要的化工原料,工业烧碱中可能含有少量NaCl。为测定工业烧碱样品中NaOH的质量分数,进行如下实验:
①称取1. 000g样品,配制成250mL待测液。
②量取20.00mL待测液,用0.1000mol/L标准盐酸溶液滴定。
(1)将1.000g样品配成250mL待测液,所用的玻璃仪器有:烧杯、玻璃棒、胶头滴管 _____________________________________;
(2)量取20.00mL待测液所用的仪器是_______________________;选用的指示剂为_____________________。
(3)滴定操作过程中,眼睛应注视____________________________________________;判断达到滴定终点的依据为_______________________________________________。
(4)第一组学生在测定时,标准盐酸滴过了头,该组学生又加了2.80mL待测液,继续做实验,这种操作__________(填:合理或不合理)。
(5)第二组学生在滴定过程中,不小心将标准液滴在锥形瓶的内壁上,一学生提议用蒸馏水将液滴冲下去,你认为这样操作使结果_______ (填:偏高、偏低或没有影响)。
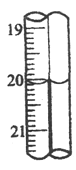
(6)第三组学生进行了两次滴定,消耗标准盐酸体积的数据如表,其中第2次滴定后滴定管的读数如图所示,将这一读数填入表中。
次数 | 滴定前(mL) | 滴定后 |
1 | 0.40 | 20.10 |
2 | 0.10 | ____________ |
该组学生所测得的烧碱样品中NaOH的质量分数为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
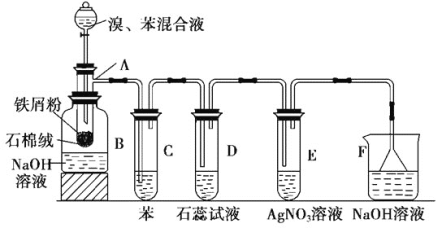
【题目】如图为苯和溴取代反应的改进实验装置。其中A为带支管的试管改制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑。
填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应。写出A中所发生反应的化学方程式(有机物写结构简式):______该反应的类型为______反应。
(2)试管C中苯的作用是_________;反应开始后,观察D试管,看到的现象为____________;
(3)在上述整套装置中,具有防倒吸作用的仪器有______(填字母)。
(4)改进后的实验除①步骤简单,操作方便,成功率高;②各步现象明显;③对产品便于观察这三个优点外,还有一个优点是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构为下图所示,这种有机物不可能具有的性质是( )
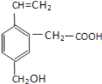
①所有碳原子可能共面;
②能使酸性KMnO4 溶液和溴水褪色,且原理相同;
③1mol 该有机物分别与足量 Na 或NaHCO3 反应,产生气体在标况下体积不相等;
④能发生酯化反应;
⑤能发生加聚反应;
⑥1mol 该有机物完全燃烧生成 CO2 和H2O 消耗 O2 的体积为 280L(标准状况)
A.①②B.②⑥C.③⑥D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钠、铝、铁是三种重要的金属。请回答:
(1)钠在空气中燃烧,得到的产物化学式为___,它的电子式为___。
(2)将一小块金属钠(2.3g)投入100mL水中,发生反应的离子方程式为__;可观察到的实验现象是__(填序号)。
a.钠沉到水底 b.钠熔成小球 c.小球四处游动
(3)向(2)所得溶液中加入5.4g铝单质充分反应,写出反应的化学方程式___,转移电子数目为___。
(4)Fe跟Cl2在一定条件下反应,所得产物的化学式是___。将该产物溶于水配成溶液,分装在两支试管中。请回答:
a.若向其中一支试管中滴加KSCN溶液,则溶液变成__色。
b.向另一支试管中滴加NaOH溶液,现象为___,反应的离子方程式是___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com