
| A. | Ba2+、AlO2-、NO3-、Cl- | B. | K+、Na+、ClO-、Fe2+ | ||
| C. | Na+、I-、NO3-、SO42- | D. | NH4+、Na+、S2-、CO32- |
分析 在碱性条件下能够大量共存,说明离子之间不发生任何反应,在强酸性条件下却能发生氧化还原反应,说明溶液中存在氧化性和还原性的离子,且在酸性条件下能发生氧化还原反应.
解答 解:A.碱性条件下离子之间不发生任何反应,酸性条件下不发生氧化还原反应,故A不选;
B.无论溶液呈酸性还是碱性,离子都不能大量共存,故B不选;
C.碱性条件下离子之间不发生任何反应,可大量共存,酸性条件下I-与NO3-发生氧化还原反应,故C选;
D.碱性条件下NH4+不能大量共存,酸性条件下不发生氧化还原反应,故D不选.
故选C.
点评 本题考查离子共存,为高考常见题型,侧重于学生的分析能力和综合运用元素化合物知识的考查,注意题目反应的特点的要求,把握离子的性质以及反应类型,答题时注意审题,难度不大.


科目:高中化学 来源: 题型:选择题
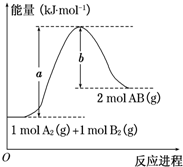 已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )
已知化学反应A2(g)+B2(g)═2AB(g)的能量变化如图所示,判断下列叙述中正确的是( )| A. | 每生成2分子AB吸收b kJ热量 | |
| B. | 该反应热△H=+(a-b)kJ•mol-1 | |
| C. | 该反应中反应物的总能量高于生成物的总能量 | |
| D. | 断裂1 mol A-A和1 mol B-B键,放出a kJ能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
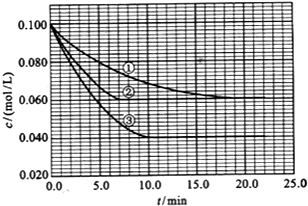 在溶液中,反应A(g)+2B(g)?C(g)分别在三种不同实验条件下进行,它们的起始浓度均为 c(A)=0.100mol/L、c(B)=0.200mol/L及c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.请回答下列问题:
在溶液中,反应A(g)+2B(g)?C(g)分别在三种不同实验条件下进行,它们的起始浓度均为 c(A)=0.100mol/L、c(B)=0.200mol/L及c(C)=0mol/L.反应物A的浓度随时间的变化如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17gNH3含有10nA个质子 | |
| B. | 标准状况下,22.4L氯水含有nA个Cl2分子 | |
| C. | 1mol C2H6含有6nA个共价键 | |
| D. | 1mol 金属K被完全氧化生成KO2,失去2nA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol苯中含有3nA个碳碳双键 | |
| B. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 一定条件下2 mol SO2和1 mol O2充分反应后,混合气体的分子总数大于2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴定管和容量瓶在使用前均需检查是否漏水 | |
| B. | 用蒸馏水湿润的pH试纸测定溶液的pH | |
| C. | 托盘天平称量药品时,都应垫上滤纸称量 | |
| D. | 石蕊、酚酞均可用作中和滴定的指示剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al是不活泼的金属,故铝可制成铝箔包装物品 | |
| B. | NaHCO3能与碱反应,故NaHCO3可以用于制作糕点 | |
| C. | NH3能与Cl2生成NH4Cl,故可用浓氨水检验输送氯气的管道是否有泄漏 | |
| D. | 明矾与K2FeO4都能与水生成胶体,均可用于水的净化、杀菌和消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 试剂 | 现象 | 结论 |
| A | 酸性KMnO4溶液 | 溶液褪色 | SO2有氧化性 |
| B | FeCl3溶液 | 溶液褪至浅绿色 | SO2有还原性 |
| C | 滴有酚酞的NaOH溶液 | 无明显变化 | SO2与NaOH溶液不反应 |
| D | 紫色石蕊试液 | 溶液变红后褪色 | SO2水溶液有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com