
| A. | C6H6 | B. | C7H8 | C. | C4H10 | D. | C3H6 |
科目:高中化学 来源: 题型:选择题
| A. | Na+、Fe2+、Cl-、SO42- | B. | K+、AlO2-、Cl-、SO42- | ||
| C. | Ca2+、Mg2+、NO3-、HCO3- | D. | Na+、Cl-、CO32-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | ②③④⑥ | C. | ②③⑤⑥ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 有X、Y、Z三种物质,它们之间存在如图转化关系:
有X、Y、Z三种物质,它们之间存在如图转化关系: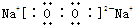 ;Y、Z两种物质相比,相同的化学键类型为离子键,当由X制取Z的上述两种途径生成Z的量相等时,转移电子数目比为1:2.
;Y、Z两种物质相比,相同的化学键类型为离子键,当由X制取Z的上述两种途径生成Z的量相等时,转移电子数目比为1:2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化硅用于制作电脑芯片和光导纤维 | |
| B. | 硫磺用于配制黑火药和工业生产硫酸 | |
| C. | 氯气用于城市自来水消毒和生产漂白粉 | |
| D. | 钾钠合金用作原子反应堆的导热剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| NaNO3 | KNO3 | NaCl | KCl | |
| 10℃ | 80.5 | 21.2 | 35.7 | 31.0 |
| 100℃ | 175 | 246 | 39.1 | 56.6 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 元素 | 相关信息 |
| X | X是形成化合物种类最多的元素,其中一种单质是自然界最硬的物质 |
| Y | Y的气态氢化物能使湿润的红色石蕊试纸变蓝 |
| Z | Z的基态原子的最外层电子排布式为ns2np4 |
| W | W的一种核素的质量数为57,中子数为31 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com