
| A、H2CO3═2H++CO32- |
| B、HClO?H++ClO- |
| C、Na2CO3=Na++CO32- |
| D、KOH=K++O2-+H+ |


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案 培优三好生系列答案
培优三好生系列答案科目:高中化学 来源: 题型:
| A、1:1 | B、5:16 |
| C、2:3 | D、3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol[Ag (NH3)2]OH配合物中含有9NA个σ键 |
| B、标准状况下,22.4L C2H6O中含C-H键5NA |
| C、1mol冰醋酸和lmol乙醇在加热和浓硫酸条件下充分反应生成的水分子数为NA |
| D、KClO3+6HCl═KCl+3Cl2↑+3H2O反应中,生成71g Cl2时,转移的电子数目为2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-859 kJ?mol-1 |
| B、+1403 kJ?mol-1 |
| C、-1718 kJ?mol-1 |
| D、-2806kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
+ 4 |
- 2 |
| A、氯化铵与KNH2反应:NH4Cl+KNH2═KCl+2NH3↑ |
| B、二价活泼金属M与液氨反应:M+2NH3═M(NH2)2+H2↑ |
| C、盐酸与MNH反应:2HCl+MNH═MCl2+NH3↑ |
| D、氯化铵与MO反应:2NH4Cl+MO═M(NH2)2+2HCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
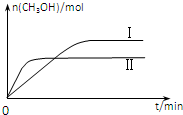 研究CO2的利用对促进低碳社会的构建具有重要的意义.
研究CO2的利用对促进低碳社会的构建具有重要的意义.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com