
在一定条件下,某化合物X受热分【解析】
2X=A↑+2B↑+4C↑
测得反应后生成的混合气体对H2的相对密度为11.43,相同条件下,X的相对分子质量是
A.11.43 B.22.85 C.80.01 D.160.02
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2015-2016学年河南洛阳高级中学高二上9月月考化学试卷(解析版) 题型:选择题
汽车尾气中,产生NO的反应为:N2(g)+O2(g) 2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是:
2NO(g),一定条件下,等物质的量的N2(g)和O2(g)在恒容密闭容器中反应,下图曲线a表示该反应在温度T下N2的浓度随时间的变化,曲线b表示该反应在某一起始条件改变时N2的浓度随时间的变化。下列叙述正确的是:
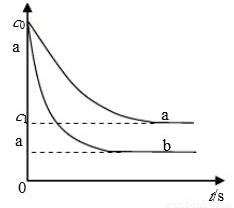
A.曲线b对应的条件改变可能是加入了催化剂
B.温度T下,随着反应的进行,混合气体的密度减小
C.温度T下,该反应的平衡常数K=
D.若曲线b对应的条件改变是温度,可判断该反应的△H<0
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上学期第一次月考化学试卷(解析版) 题型:选择题
A(g)+B(g)=C(g)△H=-Q1kJ/mol
D(g)+B(g)=E(g)△H=-Q2kJ/mol且Q1大于Q2
若A和D的混合气体1mol完全与B反应放出的热量为Q3kJ,则A与D的物质的量之比为
A.(Q2-Q1)\(Q1-Q3) B.(Q3-Q2)\(Q1-Q3)
C.(Q3-Q2)\(Q3-Q1) D.(Q1-Q2)\(Q3-Q1)
查看答案和解析>>
科目:高中化学 来源:2016届福建省莆田市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列各反应的离子方程式中,错误的是
A.硫酸铝溶液中加入过量的氨水:Al3++3NH3·H2O===Al(OH)3↓+3NH4+
B.铁片放入过量的稀硝酸中:3Fe+8H++2NO3-===3Fe2++2NO2↑+4H2O
C.将铝片放入过量NaOH溶液中:2Al+2OH-+2H2O===2AlO2-+3H2↑
D.偏铝酸钠与过量盐酸反应:AlO2-+4H+===Al3++2H2O
查看答案和解析>>
科目:高中化学 来源:2016届甘肃省高三上学期第二次检测化学试卷(解析版) 题型:选择题
氯化钠是海水的主要成分,也是人类生活中不能缺少的一种物质。下列关于氯化钠的说法正确的是
A.氯化钠溶液能导电,所以氯化钠溶液是电解质
B.氯化钠溶液可杀菌,说明氯化钠溶液具有强氧化性
C.电解熔融氯化钠和电解氯化钠溶液的产物相同
D.加碘食盐是指添加了碘的化合物的氯化钠
查看答案和解析>>
科目:高中化学 来源:2015-2016学年辽宁实验中学高一上10月阶段测化学试卷(解析版) 题型:选择题
用NA表示阿伏加德罗常数的值。下列说法中正确的是
A.2.4g金属镁变成镁离子时失去的电子数为0.1NA
B.标准状况下,11.2L CCl4所含的分子数为0.5NA
C.0.5mol/L AlCl3溶液中Cl—的数目为2NA
D.17g氨气中含有的电子数为10NA
查看答案和解析>>
科目:高中化学 来源:2016届上海市高三上学期摸底测试化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.0.1 mol组成为C2H6O的有机物,所含C—H键数目不一定为0.5NA
B.8.7 g MnO2与40 mL 10 mol/L的浓盐酸充分反应,生成的氯气分子数为0.1NA
C.0.1 mol N2与0.3 mol H2在密闭容器中,在催化剂作用下充分反应,生成氨分子数为0.2NA
D.标准状况下,22.4 L HF所含的分子数目为NA
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高一上第二次月考化学试卷(解析版) 题型:选择题
对于某些离子的检验及结论一定正确的是
A.加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO或HCO中的一种或两种
B.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
C.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,可能有Ba2+
D.加入硝酸银溶液有白色沉淀生成,则溶液中一定含有Cl-
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高一上第一次段考化学试卷(解析版) 题型:填空题
(12分)(1)常压、100℃时,等质量的SO2气体和SO3气体的密度之比为 ,原子数之比为 ,体积之比
(2)有CO与CO2的混合气体共10.8 g,标准状况下其体积为6.72L。则混合气体中二氧化碳的物质的量为 ,若混合气体缓慢通过足量的氢氧化钠溶液后,剩余的气体质量为 。
(3)将0.1 mol·L-1的K2SO4溶液、0.2 mol·L-1的Al2(SO4)3溶液和纯水混合,要使混合液中K+、Al3+、SO42-的浓度分别为0.1 mol·L-1、0.1 mol·L-1、0.2 mol·L-1,求K2SO4溶液、Al2(SO4)3溶液、纯水三者的体积比 。(忽略体积的变化)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com