
把镁条放入盛有过量稀盐酸的试管中,不影响氢气产生速率的因素是( )
A.溶液的温度 B.盐酸的浓度 C.镁条的表面积 D.加少量Na2SO4固体
科目:高中化学 来源: 题型:
下列说法正确的是( )。
①乙醇不能发生取代反应 ②甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应
③由乙酸和乙醇制乙酸乙酯与由苯甲酸乙酯水解制苯甲酸和乙醇的反应属于同一类型的反应 ④苯和乙烷都能发生加成反应
A.①②④ B.②③ C.①② D.③
查看答案和解析>>
科目:高中化学 来源: 题型:
在101kPa 25℃时,1.0g乙烷气体完全燃烧生成液态水时放出热量52.0kJ,则乙烷燃烧的热化学方程式为
A.C2H6(g) + 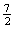 O2(g)=2CO2(g) +3H2O(l) △H =-1560kJ·mol-1
O2(g)=2CO2(g) +3H2O(l) △H =-1560kJ·mol-1
B.2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(g) △H =-1560kJ·mol-1
C.2C2H6(g) + 7O2(g)=4CO2(g) +6H2O(l) △H =+3120 kJ·mol-1
D.C2H6(g) +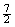 O2(g)=2CO2(g) +3H2O(l) △H =-52.0kJ·mol-1
O2(g)=2CO2(g) +3H2O(l) △H =-52.0kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
本题包括A、B 两小题,请选定其中一小题,并在相应的答题区域内作答。
若多做,则按A小题评分。
A.[物质结构与性质]
利用反应:Cu2Cl2 +C2H2+2NH3→Cu2C2(乙炔亚铜,红色)+2NH4Cl可检验乙炔。
(1)基态时亚铜离子核外电子排布式为 ▲ 。
(2)NH3中氮原子的杂化方式为 ▲ ;NH4+空间构型为 ▲ (用文字描述)。
(3)乙炔分子中σ键与π键数目之比为 ▲ ,与C22-互为等电子体的分子有 ▲ (写化学式,举一例)。
(4)氯化亚铜晶胞结构如下图,晶胞中含Cu+数目为 ▲ 。

(5)合成氨工业常用铜(I)氨溶液吸收CO生成[Cu(NH3)3(CO)]+,该配离子中配体有 ▲ (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列性质中,仅属于烷烃特征的是 ( )
A、完全燃烧产物只有二氧化碳和水 B、它们几乎不溶于水
C、分子的通式为CnH2n+2 ,与氯气发生取代反应 D、它们完全由碳氢元素组成
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( )
A.A、B、C、D、E B.E、C、D、B、A
C.B、A、D、C、E D.C、D、A、B、E
查看答案和解析>>
科目:高中化学 来源: 题型:
在周期表中,同一主族元素化学性质相似。但是也发现有些元素的化学性质和它在周期表左上方或右下角的另一主族元素性质相似,这称为对角线规则。下列有关锂及其化合物的叙述中正确的是 ( )
①锂单质跟钠单质的保存方法一样,均可保存在煤油中
②金属锂在空气中燃烧时,生成Li2O ③氢氧化锂的碱性比氢氧化铷弱
A.①② B.①③ C.①②③ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中一定能判断某化学平衡发生移动的是( )
A.混合物中各组分的浓度改变 B.正、逆反应速率改变
C.混合物中各组分的含量改变 D.混合体系的压强发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.元素周期律是元素原子核外电子排布周期性变化的结果
B.HF、HCl、HBr、HI的热稳定性和还原性从左到右依次减弱
C.第三周期非金属元素含氧酸的酸性从左到右依次增强
D.形成离子键的阴阳离子间只存在静电吸引力
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com